Review on the Determination of Oxidant Demand for in-situ Chemical Oxidation Application
-
摘要:
原位化学氧化(ISCO)修复技术由于修复周期短、效率高等特点已被广泛应用于土壤和地下水的有机污染修复。ISCO修复中所需的氧化剂的剂量通常用氧化剂需求量来衡量,在实际应用过程中,使用的氧化剂剂量过多或过少均会产生一定的负面影响。因此,氧化剂需求量的准确测算对于获得良好的工程修复效益具有重要意义。本文在对氧化剂需求量的组成及定义进行梳理、统一的基础上,重点综述了相关测算方法的原理和应用现状。ISCO修复中总氧化剂需求量(TOD)的组成包括污染物氧化剂需求量(POD)、天然氧化剂需求量(NOD)和氧化剂分解量(DEO)。NOD和DEO的存在为有机污染物有效的修复降解和TOD的准确测算带来了挑战。氧化剂需求量的测算方法可以分为实验法和化学计量模型法两大类,实验法又可以分为批实验法、柱实验法、注抽实验法和反应动力学模型法,批实验法的是目前应用目前较为最为广泛。在实验法中,同一样品的不同时间点获得的氧化剂需求量差距可以达到37%,因此应把污染物浓度在氧化作用下降低到目标限值所需要的时间作为氧化剂需求量的测定时间,并且为了更为精准地提供氧化剂需求量,有必要使用带有测试条件的表达方式来进行表示。目前的氧化剂需求量测算方法多针对于高锰酸钾氧化剂需求量。芬顿试剂和臭氧等分解性较强的氧化剂的DEO可能达到TOD的50%以上,现有方法对DEO的准确测算仍面临困难,应予以特别关注。除了需要开发出能够准确获得DEO的测算方法,场地施工条件对TOD的影响也需要进一步探究,氧化剂需求量的测算仍需一个更为科学的工作流程或指南。
要点(1) 氧化剂需求量的测算方法包括实验法和化学计量模型法,实验法中的批实验法由于简便、高效受到了较为广泛的关注与应用。
(2) 现有测算方法缺乏对高锰酸钾氧化剂外的其他种类氧化剂需求量测算的验证和探索。
(3) 对于分解性较强的氧化剂,氧化剂分解量(DEO)对总氧化剂需求量(TOD)的测算具有重要影响。
HIGHLIGHTS(1) The determination of oxidant demand includes two categories: experimental method and stoichiometric model method. The experimental method of batch testing has been more widely used because of its simplicity and efficiency.
(2) There is a lack of validation and exploration of existing determination for measuring the oxidant demand for oxidants other than potassium permanganate.
(3) Decomposed oxidant (DEO) has an important effect on the total oxidant demand (TOD) determination for those oxidants with strong decomposition ability.
Abstract: In-situ chemical oxidation (ISCO) refers to the use of appropriate conveyance technology to transport oxidants into soil or aquifer, where the contaminants are converted to low- or non-toxic substances by chemical oxidation. ISCO has been widely used for the remediation of organic contaminants in soil and groundwater due to its high efficiency and cost effectiveness.Oxidant demand is an important parameter in the application of ISCO. Once injected into the contaminated soil or aquifer, the oxidant reacts not only with the target contaminants, but also with natural organic matter (NOM) and reductive minerals (RM) such as Fe2+, Mn2+, S- and S2- in the medium. In addition, the oxidant may decompose naturally due to its own properties. If the amount of oxidant used is insufficient, the remediation of the contaminated site may not meet the project objectives and residual contaminants or reaction intermediates may be formed, resulting in a rebound of the contaminant concentration at the site. If too much oxidant is used, it would not only increase the cost of remediation, but also seriously damage the physical and chemical properties of soil, reducing the diversity of microbial communities. Therefore, accurate measurement of oxidant requirements is important to achieve good remediation performance.In previous studies, the specific meaning of terms related to oxidant demand is not consistent and they are often mixed in different studies, which would lead to ambiguity.In this review the composition and definition of oxidant demand is clarified and unified. The total oxidant demand (TOD) in ISCO is composed of pollutant oxidant demand (POD, the amount of oxidant consumed by oxidative degradation of pollutants), natural oxidant demand (NOD, the amount of oxidant consumed by natural organic matter and reducing minerals in soil or aquifer media), and decomposed oxidant (DEO, the amount of oxidant naturally decomposed due to its nature and the influence of environmental conditions).The methods for determining oxidant demand can be divided into two categories: experimental method and stoichiometric model method. The basic principle of the experimental method is to mix the treated medium sample with the oxidant in a system for a period of time, and then calculate the oxidant consumption before and after reaction to obtain the oxidant demand per unit of medium. Specifically, the experimental method can be divided into batch test, column test, push-pull test and reaction kinetics model according to the scale and dimension of the experiment. Among them, the batch test has been relatively widely used due to its excellent characteristics of simplicity and efficiency. The column test is more capable of reflecting the actual consumption of oxidant in the field medium, taking into account the transport process and interaction of oxidant in porous media. Although the push-pull test is carried out at the field scale, which can effectively overcome the error caused by the difference between laboratory conditions and field conditions, it is relatively complex to operate. Finally, the reaction kinetics model can be used to analyze the oxidant consumption in the reaction process based on experiments. This method can characterize the oxidant consumption on a longer time scale, which is of great importance for potassium permanganate or sodium persulfate oxidants with longer reaction times.The determination of oxidant demand by experimental method is affected by factors such as the initial concentration of oxidant, reaction time, solid-to-liquid ratio and mixing conditions of the reaction. To facilitate comparison of data and costing of the project, it is necessary to incorporate experimental conditions into the expression of oxidant demand. For example, the difference of the oxidant demand obtained at different times for the same sample can be as much as 37%. Therefore, the time required for the pollutant concentration to be reduced to the target limit by oxidation should be used as the oxidant demand determination time.Stoichiometric model method is the determination of the theoretical oxidant demand value by the establishment of the stoichiometric relationship model between the oxidant demand and the components in the medium. The stoichiometric model method was originally designed to explore the relationship between the total organic carbon in the medium and the oxidant demand. It was then developed to consider the oxidant demand of natural organic matter, other mineral ions and organic pollutants as a whole. Calculation results of the stoichiometric modelling method depend on the accuracy of the model and the precise determination of the content of relevant components in the medium.Both experimental method and stoichiometric model method mostly take potassium permanganate oxidant as the research object, but there is a lack of research on the demand of Fenton reagent, ozone and sodium persulfate. In particular, the DEO of more decomposable oxidants such as Fenton reagent and ozone may reach more than 50% of TOD. The existing methods still face difficulties in accurately measuring DEO, which deserves special attention. As a component of TOD that is easily overlooked, the importance of DEO needs to be further clarified and more accurate measurement methods need to be explored. In the actual project, the number of injection wells, well spacing, oxidant injection rate and other design parameters will have an important impact on the total oxidant demand, which still needs to be further investigated. The remediation of contaminated sites by ISCO is a complex project and a more scientific workflow or guideline is necessary for engineers to determine oxidant demand.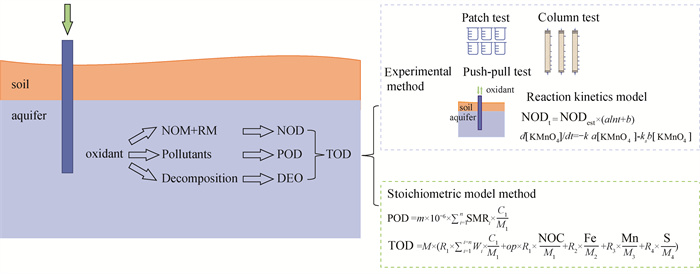
-
原位化学氧化(In-situ Chemical Oxidation,ISCO)是指利用合适的输送技术将氧化剂输送到土壤或含水层中,通过化学氧化作用将污染物转化为低毒或者无毒物质,由于反应高效、性价比高等特点,ISCO修复技术已经在土壤和地下水的有机污染修复中得到了广泛应用[1-3]。氧化剂用量是应用中的一个关键参数,当氧化剂用量不足时,污染场地的修复可能达不到工程的目的要求,易形成残留污染物或反应中间产物,导致场地污染物浓度发生反弹[3-6];当氧化剂用量过多时,则可能会严重破坏土壤理化性质,降低微生物群落的多样性,增加工程的修复成本[7-12]。因此,ISCO中所使用的氧化剂剂量的准确测定是确定污染场地治理效果的关键,对于最终获得良好的修复效益具有重要的意义[13]。
ISCO工程中所需氧化剂的剂量通常用氧化剂需求量来衡量。经过调研总结,目前针对氧化剂需求量的测算方法可以划分为实验法和化学计量模型法两类[14-15],实验法又可以分为批实验法、柱实验法、注抽实验法以及基于这三者的反应动力学模型法[7-8, 16]。在不断的发展实践中,实验法中的批实验法得到了较为广泛的探索,尤其是美国材料试验协会(ASTM)提出的相关标准(D7262)有力促进了其标准化的应用。化学计量模型法则直到近年来与Li等[13]和Ranc等[14]提出了新的模型才有了较大的发展。
然而,上述方法的研究依然存在不足:一是相关概念定义不统一,不同文献中术语定义不同;二是缺乏对不同种类的氧化剂需求量的考量,当前氧化剂需求量的测定方法主要针对高锰酸钾氧化剂,对其他种类的氧化剂的探究还相对较少;三是对氧化剂自然分解量的测算研究还略有不足。本文根据国内外研究现状,对氧化剂需求量的组成及定义进行讨论和梳理,在此基础上,对各种氧化剂需求量测算方法的使用特点和应用现状进行了综述,同时对当前方法在不同氧化剂种类条件下的应用、氧化剂自然分解量的测算进行了一定探讨。相关内容有助于人们了解氧化剂需求量测算方法的原理与现状,并为今后开展相关研究提供依据和建议。
1. 氧化剂需求量的组成与定义
当氧化剂被注入到受污染的土壤或含水层之后,氧化剂除了与目标污染物发生反应,同时还与介质中的天然有机质(Natural Organic Matter,NOM)以及Fe2+、Mn2+、S-、S2-等还原性矿物质(Reductive Mineral,RM)发生反应[16-20],并且伴随着由于氧化剂自身性质而发生的自然分解,如芬顿试剂和臭氧会分解成氧气等[21]。为了更好地表示氧化剂需求量的组成,研究者使用了许多术语,如总氧化剂需求量(Total Oxidant Demand,TOD)[7, 21-24]、土壤氧化剂需求量(Soil Oxidant Demand,SOD)[13, 18, 25-27]、天然氧化剂需求量(Natural Oxidant Demand,NOD)[7-9, 15, 16, 21-24, 28-30]以及氧化剂分解量(Decomposed Oxidant DEO,DEO)[17, 21, 24, 29]等。这些术语具体含义尚不统一,易产生歧义,常常在不同的研究中被混用。例如,由于SOD未明确是否包含土壤中的污染物对氧化剂的需求量,常常与TOD或NOD混用。
本文根据已有术语的定义及使用情况,进一步考虑介质类型和氧化剂消耗的组成,将相关术语关系及定义梳理总结列于表 1。同时明确SOD指的是土壤中的天然有机质和矿物质所消耗的氧化剂剂量,它是NOD的一部分,也可以称为土壤的NOD。
表 1 氧化剂需求量相关术语及定义Table 1. Terms and concepts related to oxidant demand氧化剂需求量相关术语 定义 污染物氧化剂需求量
(Pollutant Oxidant Demand,POD)污染物氧化降解所消耗的氧化剂量 天然氧化剂需求量
(Natural Oxidant Demand,NOD)土壤或含水层介质中的天然有机质和还原性矿物质所消耗的氧化剂量 氧化剂分解量
(Decomposed Oxidant, DEO)氧化剂因本身的性质以及环境条件的影响而自然分解,未能参与到氧化反应过程中的那部分剂量 需要特别指出的是,表 1所列术语的单位统一为g、kg或mol氧化剂,而非前人文献中通常使用的氧化剂需求量单位:g氧化剂/kg介质,因为绝大部分前人的研究中氧化剂的需求量都是针对单位质量介质而言的。如Dangi等[31]通过总结指出,单位质量土壤的高锰酸钾NOD可以达到0.4~50.0g/kg。研究者们还指出,介质中的天然物质可能比污染物对氧化剂的需求更高[32],它们之间的竞争可能对氧化剂的用量、扩散程度、氧化反应速率以及污染物的去除效率产生显著影响[7, 14, 20, 28, 33-36]。因此,POD和NOD的测算均受到了研究者们的重视,而对于DEO,目前的测算方法对其关注尚且不足。本文在对现有测算方法进行综述的基础上,对DEO的测算进行了一定探讨。
2. 实验法测算氧化剂需求量
实验法是较为经典的氧化剂需求量测算方法,基本原理是:将经过粉碎、干燥及其他方法处理的介质样品与氧化剂在一定体系内混合反应一段时间,通过计算反应前后氧化剂的消耗量进而得到单位介质的氧化剂需求量。其基本的数学表达式为:
$$ \mathrm{NOD}_{\mathrm{t}} / \mathrm{TOD}_{\mathrm{t}}=\frac{\left(C_1-C_2\right) \times V}{m_{\mathrm{s}}} $$ (1) 式中:C1、C2分别表示反应前后氧化剂浓度,单位为g/L;V表示加入的氧化剂溶液体积,单位为L;ms表示介质样品质量,单位为kg;t表示时间,单位为小时(h)或天。需要指出的是,由于并未特别考虑氧化剂的DEO,此处的TOD指的是POD和NOD之和,单位均为:g氧化剂/kg。在该基础上,场地总NOD值或总TOD值则还需乘以污染区域介质的总质量。
根据实验的尺度和维度的逐渐增加,实验法可以分为批实验法、柱实验法和注抽实验法,以及基于上述三种方法,利用动力学模型预测更长时间尺度上的氧化剂需求量的反应动力学模型法。
2.1 批实验法
Haselow等[7]提出利用比色技术(Colorimetric Techniques)来估算单位土壤或含水层的TOD,该方法实质上就是基于上述原理的批实验法(Batch Test)。经过不断发展,ASTM[15]提出了测算单位质量土壤或含水层固体的高锰酸钾天然氧化剂需求量的标准试验方法。王文坦等[37]提出了土壤的化学需氧量的测定方法专利,促进了批实验法在国内外的标准化应用。批实验法具有操作简便、高效、对不同场地介质和不同的氧化剂种类适应性较强等特点,在许多污染修复研究中得到运用[25, 27, 38-39]。
批实验法的结果受到许多因素的影响,包括氧化剂的初始浓度、反应时间、反应的固液比以及反应的混合条件等。前人对批实验中相关影响因素及影响机制进行了大量探究,可以总结得出:更高的氧化剂浓度和更长的反应时间意味着氧化剂与污染物之间更充分的反应,但这也带来了更高的氧化剂消耗[13, 31];固液比对实验的影响与氧化剂是否充足以及反应时间有关[21, 31];搅拌混合可以促进氧化剂与土壤含水层介质充分反应[31],但可能不符合实际的应用情况,因为在实际条件下氧化剂与介质的接触并没有这样充分。为了便于不同研究或修复工程数据的对比,支撑工程的成本核算,根据实验影响条件,批实验中NOD或TOD科学的表达方式应该为特定样品与一定浓度的特定氧化剂,在一定的固液比、温度和混合条件下反应一定时间时的氧化剂的消耗量,并且某一场地某一氧化剂的NOD或TOD应该是一组数据。因此,比较严谨的氧化剂需求量的表述方式为:NOD/TOD(XX浓度YY氧化剂,固液比,反应温度,反应时间,混合条件)。例如,NOD(0.5mol/L KMnO4,1∶5,25℃,48h,充分混合),表示使用0.5mol/L的高锰酸钾溶液,固液比为1∶5,反应温度为25℃,反应时间为48h,充分混合条件下的天然氧化剂需求量。同理,柱实验和注抽实验测算值的表达也应是如此,只是需要考虑的因素有所差别。
研究者们在利用批实验法测算高锰酸钾的氧化剂需求量时发现,氧化剂的消耗速率在一定时间后会发生显著降低,尔后呈现出较长时间的缓慢消耗,即存在钝化现象和拖尾现象。发生钝化现象的所需时间随着高锰酸钾浓度升高而变短,拖尾现象则可以持续到14天以上[31]。Xu等[40]指出,钝化现象与高锰酸钾氧化剂的特征产物MnO2生成有关。拖尾现象则可能是由于介质中部分反应物与氧化剂反应较慢,或是吸附在介质上的相关还原性物质解吸较慢。钝化现象和拖尾现象的存在延长了实验的时间,使得氧化剂需求量的测算变得困难、复杂。ASTM的标准方法中是以48h处的氧化剂消耗量作为测定值,根据钝化现象和拖尾现象,这具有一定风险[6],因为此时获得的氧化剂消耗量可能并未达到最高。在不同反应时间条件下,氧化剂的消耗量可能有较大差距。如Dangi等[31]的测试结果表明,在高氧化剂浓度下,48h和14天时所获得的高锰酸钾NOD值相差可以达到前者的37%。如果等待氧化剂与样品反应完全、氧化剂消耗量达到相对稳定,则可能需要耗费较长的时间。考虑到ISCO工程的主要目的是有效地降低污染物的浓度,实验时间不应该是一个固定的时间,而应是污染物浓度在氧化作用下降低到目标值以下所需要的时间。Xu等[41]提出了一种改进的方法用于测定样品的NOD或TOD最大值,即对介质样品进行了进一步的酸化、加热等处理,以促进介质中的物质与高锰酸钾发生更加充分、快速的反应,避免拖尾现象。该方法所得的测算值是介质中的物质完全氧化所需的氧化剂的剂量,ISCO工程可能并不需要完全满足天然物质对氧化剂的需求[22]。因此,上述方法的测算值可能偏大。
批实验法已经得到了较为广泛的研究和实践,但还具有进一步优化的空间。由于具有简便、高效的显著优势,该方法将仍然是最受青睐的氧化剂需求量测算方法。批实验法可以显示出氧化剂需求量与时间的变化关系,而柱实验法在此基础上可以进一步模拟氧化剂在介质中实际运输中的氧化剂消耗。
2.2 柱实验法
柱实验(Column Test)的大致方法是:将场地介质填充到实验柱中,通入一定浓度的氧化剂,观察氧化剂浓度在时间和空间上的双重分布,通过流经实验柱前后氧化剂含量的变化获得NOD或TOD值。氧化剂含量的变化可通过反应前后氧化剂浓度变化获得[42],也可以通过对穿透曲线的积分来获得[8]。在柱实验中,氧化剂与介质之间的固液比、混合条件将不再是实验所考虑的重要因素。而氧化剂浓度和反应时间的影响机制则与批实验中相同[43]。Xu等[44]研究发现,从柱实验中测得的高锰酸钾NOD值是批试验中7天时所测得的NOD值的0.1~0.5倍,这说明批实验和柱实验法的测算结果可能有较大差异。由于考虑了氧化剂的流动运输,氧化剂与介质之间的接触更加符合实际情况,柱实验被认为更能够反映出氧化剂在场地介质中的实际消耗[8, 44]。
尽管柱实验法的准确性具有一定优势,但该方法并未得到广泛的研究应用,也未形成较为清晰的操作和计算流程。推测造成这一现象的主要原因是柱实验的操作和计算都较为繁琐和复杂。如当介质非均质性较强导致所需测定的样品较多时,工作量和实验成本将显著增加。在这样的背景下,柱实验的下一步发展方向应是形成较为完整的工作流程,同时进一步探究与批实验测算值之间的联系或差异。
2.3 注抽实验法
Mumford等[16]提出使用注抽实验(Push-Pull Test,PPT)来测定含水层介质的NOD。注抽技术起源于石油工业,主要用途是确定介质中的剩余油饱和度、介质水文地质参数[45],后来被广泛用于地下水的原位修复中,尤其对于场地中非水相液体(NAPL)污染的修复具有重要意义[46]。通过该方法测算氧化剂需求量的主要操作是:通过注入装置将已知含量的氧化剂和示踪剂混合注入到含水层中,在经过一段时间的反应后测定剩余氧化剂的含量,通过反应前后的差值进而估算含水层介质的NOD或TOD[16]。其中,示踪剂用来控制样品的回收率。该方法的基本原理与2.1中所述原理相同,由于在场地尺度上进行,因此也可以称为场地实验或是中试实验[47]。Ko等[48]利用简单的单井注抽试验对ISCO工程场地中TCE的降解率和高锰酸盐的消耗率进行了估算,显示出了较好的适用性。Mathai[46]设计了数值模型“PPT-ISCO”来模拟注抽试验,用于评估天然氧化剂需求量大小和ISCO的有效性,并且探究了注抽实验在NAPL相污染物修复效果调查和氧化剂需求量测算中的应用,推动了注抽实验法的数值模拟应用。
目前,注抽实验法的应用并不广泛。其主要优点在于可以有效地克服实验室条件与实际场地环境条件不同所导致的误差,获得比实验室试验更具代表性的测定值[46],可以在场地原有的监测井中进行以节约部分成本[16]。但同时,该方法的大规模使用仍面临一些困难:一是其准确性依赖于对与氧化剂发生接触的含水层介质体积和质量的准确估算;二是当场地介质条件或污染物分布较为复杂时,需要进行多次实验;三是该方法适用于含水层介质,对于土壤非饱和带的适用性还有待进一步的验证。尽管如此,注抽实验法对于验证氧化剂需求量的实验室测算结果以及探究NAPL污染源区的氧化剂需求量仍具有重要意义。在进行ISCO设计时,柱实验和注抽实验通常会被用来探究氧化剂的输送以及实际的氧化修复效果,可以在进行这些探究的同时考虑进行氧化剂需求量的测算,进而避免更多的操作和成本消耗,将有利于促进两种方法的发展与应用。
2.4 反应动力学模型法
反应动力学模型法(Reaction Kinetics Model)是指在实验基础上,对反应过程中氧化剂的消耗量进行动力学分析,从而能够在更长的时间尺度上刻画氧化剂的消耗,这对于反应时间较长的高锰酸钾或过硫酸钠氧化具有较大的意义。Mumford等[8]在批、柱实验的基础上提出了t时刻高锰酸钾NOD值与理论NOD最大值之间的关系拟合模型:
$$ \mathrm{NOD}_{\mathrm{t}}=\mathrm{NOD}_{\text {est }} \times(a \ln t+b) $$ (2) 式中: NODest为利用化学计量模型计算的理论最大值,将在化学计量模型法中介绍,a和b为拟合参数。Xu等[40]给出了高锰酸钾反应NOD最大值与7天时测得的NOD值之间的关系模型,式中的NODmax是根据反应动力学图像估算出的最大值:
$$ \mathrm{NOD}_{\max }=1.5 \times \mathrm{NOD}_7+0.7 $$ (3) 上述模型能够帮助人们在不需要进行长时间的实验情况下估算介质的NOD最大值,具有使用简便的优势,但需要考虑适用的氧化剂浓度等条件。ASTM的标准中给出的基于实验室测定的高锰酸钾消耗的一级动力学模型[15],该模型考虑到了高锰酸钾氧化反应的钝化,并将反应过程划分为快速反应和缓慢反应两个阶段,两个阶段的分界点为反应速率变化的拐点。最终表达式为:
$$ \mathrm{d}\left[\mathrm{KMnO}_4\right] / \mathrm{d} t=-k_{\mathrm{f}} a\left[\mathrm{KMnO}_{4 \mathrm{f}}\right]-k_{\mathrm{s}} b\left[\mathrm{KMnO}_{4 \mathrm{s}}\right] $$ (4) 式中:[KMnO4f]和[KMnO4s]分别为快速反应和缓慢反应阶段的KMnO4浓度;kf和ks分别为快速反应和缓慢反应的阶段一级反应动力学常数;a和b分别表示参与快速反应阶段和缓慢反应阶段的KMnO4的质量占总质量的比例,可以通过测定反应初始KMnO4质量以及拐点处KMnO4的质量来确定。该模型的主要优点是标准化,缺点是使用成本相对较高。
反应动力学模型法目前仅被用来估算介质的NOD。除此之外所面临的主要问题是,现有模型在不同实验条件下的适用性尚不明确,同时缺乏对高锰酸钾之外的氧化剂的研究,这都应是其进一步发展的方向。
综上所述,由于简便、高效的突出特点,批实验法是目前最受关注、应用最为广泛的氧化剂需求量测算方法,但由于主要针对的是高锰酸钾氧化剂,尽快推出针对其他种类氧化剂的标准方法是当前较为迫切的工作。而柱实验法和注抽实验法被认为更能代表氧化剂的实际消耗,进一步探究并量化三种方法测算结果的差异性、推出柱实验法和注抽实验法的标准实施流程将是下一步工作的难点。
3. 化学计量模型法测算氧化剂需求量
化学计量模型法是指通过建立氧化剂需求量与介质中各个组分之间化学计量关系模型来得到理论的氧化剂需求量值。化学计量模型法的初期探索是探究介质中总有机碳与氧化剂需求量之间的关系。如Hendrych等[49]指出,天然介质的高锰酸钾NOD与介质中的有机碳含量在很大范围内呈线性关系,Xu等[40]提出了利用有机碳含量计算NOD的经验模型。在不断发展中,研究者们进一步关注到有机污染物以及介质中的还原性矿物对氧化剂的需求。Ranc等[14]提出了针对介质中多环芳烃污染物的POD的计算模型(原文中用化学计量需求量(Stoichiometric Oxidant Demand,SOD)表示,单位为mol):
$$ \mathrm{POD}=m \times 10^{-6} \times \sum\limits_{i=1}^n \mathrm{SMR}_i \times \frac{C_i}{M_i} $$ (5) 式中:Ci和Mi分别代表第i种多环芳烃化合物的浓度(mg/kg)和摩尔质量,m指介质质量,SMRi指氧化剂与污染物之间的化学计量摩尔比(Stoichiometric Molar Ratio),即理论上将1mol目标污染物氧化为二氧化碳所需的氧化剂的摩尔质量,一般通过化学反应方程获得。该模型的显著优势是被证明可以在不同氧化剂种类条件下使用,如Bendouz等[50]利用式(5)计算了芬顿试剂和过硫酸钠降解污泥中多环芳烃污染物的POD。
Li等[13]统筹考虑了天然有机质和其他矿物离子以及有机污染物的氧化剂需求量,提出单位介质的TOD计算模型:
$$ \begin{aligned} \mathrm{TOD}_{\text {est }}= & M \times\left(R_1 \times \sum\limits_{i=1}^n W_i \times \frac{C_i}{M_1}+o p \times R_1 \times \frac{\mathrm{NOC}}{M_1}+\right. \\ & \left.R_2 \times \frac{\mathrm{Fe}}{M_2}+R_3 \times \frac{\mathrm{Mn}}{M_3}+R_4 \times \frac{\mathrm{S}}{M_4}\right) \end{aligned} $$ (6) 式中:M、M1、M2、M3、M4分别代表KMnO4、碳、铁、锰、硫元素的摩尔质量;R1、R2、R3、R4分别代表KMnO4获得的电子数与被氧化原子失去的电子数之比;op为天然有机质的最大氧化率,与KMnO4浓度有关;n为有机污染物种类数;NOC为天然有机碳的含量(g/kg),TODest表示单位介质理论计算的TOD最大值。Ci和Wi分别代表第i种污染物的浓度(g/kg)和碳的质量分数;Fe、Mn和S分别代表背景土壤中铁、锰和硫的浓度(g/kg)。
通过对式(6)中组分的选择,可以实现对NOD或POD理论值的计算。该模型的提出基于两个基本的假设:一是氧化剂与介质、污染物充分接触;二是有机物、还原性矿物与氧化剂完全反应[13]。在这样的假设下,测算值将不可避免地偏大,因此在计算NOD时可以与式(2)联立来获得更贴合实际的NOD值。
化学计量模型法的测算结果依赖于模型的准确性以及对介质中相关组分含量的准确测定。与实验法相比,化学计量模型法可以有效地避免实验因素对结果的影响,对于不同的场地介质也具有较好的适用性。它作为一种简便、高效、经济的氧化剂需求量测算方法,具有较好的应用前景。但同时,该方法需要进一步探索在其他种类的氧化剂条件下的适用性,并在更多的实际应用中加以论证。
4. 不同种类氧化剂需求量和氧化剂分解量的测算方法现状
无论是实验法还是化学计量模型法,多以高锰酸钾氧化剂作为研究对象,缺乏对芬顿试剂、臭氧以及过硫酸钠等氧化剂需求量的探究。
批实验法已经被应用到过硫酸钠氧化剂需求量的测定中[37, 51]。Liu等[20]利用批实验探究了过硫酸钠降解氯化挥发性有机化合物时与土壤介质的相互作用,发现土壤的过硫酸钠NOD值可以达到16.8~40.2g/kg,占据了TOD的较大比重。Dangi等[32]也利用批实验法进行评估发现,由于在高浓度条件下会发生活化而导致更充分的氧化反应,过硫酸钠NOD值在低浓度和高浓度下的差别明显比其他氧化剂高。因此,未来批实验法研究中需要特别关注不同活化条件下的过硫酸钠氧化剂需求量的测算,而其他实验法以及化学计量模型法的应用则都还有待进一步的发展和实践。
对于芬顿试剂与臭氧等分解性较强的氧化剂,DEO可能成为TOD的重要组成部分。如Baciocchi[36]指出芬顿试剂由于歧化反应产生的DEO可达到TOD的50%以上;高锰酸钾和过硫酸钠等氧化剂尽管分解性不强,但如果场地修复时间较长,则其DEO可能不能轻易忽略。对于过硫酸钠与高锰酸钾的分解量的测算,在实验法测算过程中伴随着氧化剂的自然分解,因此DEO实则已经被考虑在内。而对于芬顿试剂和臭氧,两者的自然分解半衰期一般以小时计,分解速率较高,与物质反应的速率较快,并且分解产生气体或本身是气体,为实验法测算带来了很大挑战。如王文坦等[37]提出的批实验法专利中指出,该专利适用于溶质质量分数在10%以下的芬顿试剂或过氧化氢溶液。而Xu等[52]通过进行批、柱实验指出,由于较大的固体质量与溶液体积比,芬顿试剂柱实验中分解速率常数比在批实验中更高,说明两种方法测得的NOD值可能有较大差异。这意味着将芬顿试剂氧化剂需求量的批实验测定值直接应用到实际中去必须谨慎,需要进一步的探索和验证。除此之外,DEO的刻画难点还在于会受到氧化剂注入速率、注射井设置等项目施工状况的影响。例如,在利用注射井注射氧化剂时,如果注入浓度和注入速率较高,会在注射井附近产生高温区域,可能会造成氧化剂的大量分解[21]。
除了批实验法,柱实验法、注抽实验法的操作均更加复杂,而化学计量模型法则是未考虑氧化剂的自然分解,因此可行性均有待发展验证。考虑到各方法的应用现状,本研究较为推荐利用注抽实验法进行估算,即不苛求进行准确的测算,在缓慢注入氧化剂的同时测定污染物的含量,当含量降至目标值以下时,以此时的氧化剂输入量为测定值,进行场地TOD的估算。该方法可以在进行氧化剂的修复效果的场地中试实验中进行。在实际的ISCO工程应用中,更受关注的可能依然是如何控制芬顿试剂和臭氧的氧化和分解速度。
5. 结语与展望
本文在对氧化剂需求量的组成和定义进行梳理的基础上,对比阐述了不同的氧化剂需求量测算方法的特点和使用现状。研究发现,原位化学氧化(ISCO)中总氧化剂需求量(TOD)由污染物氧化剂需求量(POD)、天然氧化剂需求量(NOD)和氧化剂分解量(DEO)三部分构成,氧化剂需求量的测算方法主要包括实验法和化学计量模型法,实验法中的批实验法的应用最为广泛,而化学计量模型法经过不断的发展,表现出了较大的应用潜力。考虑到实验法中不同时间点获得的氧化剂需求量的差异,提出把污染物浓度在氧化作用下降低到目标限值所需要的时间作为氧化剂需求量的测定时间,同时使用带有测试条件的表达方式从而更精准地提供氧化剂需求量。目前的氧化剂需求量测算方法对高锰酸钾、过硫酸钠等分解性较低的氧化剂表现出较好的适用性,而对于芬顿试剂和臭氧等分解性较强的氧化剂,则由于DEO占据TOD的较大比重,准确测算仍面临困难。
作为容易被忽略的TOD的组成部分,DEO的重要性需要进一步明确,同时探索更准确的测算方法。在实际工程中,注入井数量、注入井间距、氧化剂注入速率等施工参数都会对总的氧化剂需求量产生影响,需要进一步的探究。原位化学氧化修复污染场地是一个复杂的工程,氧化剂需求量的测算仍需一个更为科学的工作流程或指南。
-
表 1 氧化剂需求量相关术语及定义
Table 1 Terms and concepts related to oxidant demand
氧化剂需求量相关术语 定义 污染物氧化剂需求量
(Pollutant Oxidant Demand,POD)污染物氧化降解所消耗的氧化剂量 天然氧化剂需求量
(Natural Oxidant Demand,NOD)土壤或含水层介质中的天然有机质和还原性矿物质所消耗的氧化剂量 氧化剂分解量
(Decomposed Oxidant, DEO)氧化剂因本身的性质以及环境条件的影响而自然分解,未能参与到氧化反应过程中的那部分剂量 -
[1] 郑伟, 梅浩, 陈敬仁. 原位化学氧化技术在地下水修复工程中的应用[J]. 资源节约与环保, 2018(10): 23-25. doi: 10.3969/j.issn.1673-2251.2018.10.026 Zheng W, Mei H, Chen J R. Application of in situ chemical oxidation technology in groundwater remediation projects[J]. Resources Economization & Environmental Protection, 2018(10): 23-25. doi: 10.3969/j.issn.1673-2251.2018.10.026
[2] 沈宗泽, 王祺, 阎思诺, 等. 连续管式原位注入化学氧化技术对某有机污染场地地下水的修复效果[J]. 环境工程学报, 2022, 16(1): 93-100. https://www.cnki.com.cn/Article/CJFDTOTAL-HJJZ202201010.htm Shen Z Z, Wang Q, Yan S N, et al. Pilot scale study on groundwater remediation in an organic contaminated site by coiled tubing in situ injection chemical oxidation technique[J]. Chinese Journal of Environmental Engineering, 2022, 16(1): 93-100. https://www.cnki.com.cn/Article/CJFDTOTAL-HJJZ202201010.htm
[3] 章生卫, 程小谷, 于李罡, 等. 石油烃污染地下水原位化学氧化修复研究[J]. 环境科学与技术, 2021, 44(S1): 56-60. doi: 10.19672/j.cnki.1003-6504.2021.S1.009 Zhang S W, Cheng X G, Yu L G, et al. Research on in situ chemical oxidation remediation of groundwater contaminated by petroleum hydrocarbons[J]. Environmental Science & Technology, 2021, 44(S1): 56-60. doi: 10.19672/j.cnki.1003-6504.2021.S1.009
[4] Boulangé M, Lorgeoux C, Biache C, et al. Fenton-like and potassium permanganate oxidations of PAH-contaminated soils: Impact of oxidant doses on PAH and polar PAC (polycyclic aromatic compound) behavior[J]. Chemosphere, 2019, 224: 437-444. doi: 10.1016/j.chemosphere.2019.02.108
[5] 曹兴涛, 谷广锋, 王新新, 等. 储油罐污染场地原位化学氧化修复进展[J]. 现代化工, 2017, 37(6): 20-23. doi: 10.16606/j.cnki.issn0253-4320.2017.06.005 Cao X T, Gu G F, Wang X X, et al. Progress of in situ chemical oxidation remediation of contaminated site by leaking oil storage tank[J]. Modern Chemical Industry, 2017, 37(6): 20-23. doi: 10.16606/j.cnki.issn0253-4320.2017.06.005
[6] Huling S G, Ross R R, Prestbo K M. In situ chemical oxidation: Permanganate oxidant volume design considerations[J]. Groundwater Monitoring & Remediation, 2017, 37(2): 78-86.
[7] Haselow J S, Siegrist R L, Crimi M, et al. Estimating the total oxidant demand for in situ chemical oxidation design[J]. Remediation Journal, 2003, 13(4): 5-16. doi: 10.1002/rem.10080
[8] Mumford K G, Thomson N R, Allen-King R M. Bench-scale investigation of permanganate natural oxidant demand kinetics[J]. Environmental Science & Technology, 2005, 39(8): 2835-2840.
[9] Kim U, Parker J C, Borden R C. Stochastic cost-optimization and risk assessment of in situ chemical oxidation for dense non-aqueous phase liquid (DNAPL) source remediation[J]. Stochastic Environmental Research and Risk Assessment, 2019, 33(1): 73-89. doi: 10.1007/s00477-018-1633-y
[10] Kakosová E, Hrabák P, Cerník M, et al. Effect of various chemical oxidation agents on soil microbial communities[J]. Chemical Engineering Journal, 2017, 314: 257-265. doi: 10.1016/j.cej.2016.12.065
[11] 杨乐巍, 张岳, 李书鹏, 等. 原位化学氧化高压注射修复优化设计与应用案例分析[J]. 环境工程, 2019, 37(8): 185-189. https://www.cnki.com.cn/Article/CJFDTOTAL-HJGC201908034.htm Yang L W, Zhang Y, Li S P, et al. A case study on design and application of in situ chemical oxidation high pressure injection remediation[J]. Environmental Engineering, 2019, 37(8): 185-189. https://www.cnki.com.cn/Article/CJFDTOTAL-HJGC201908034.htm
[12] Wang N, Zheng T, Zhang G, et al. A review on Fenton-like processes for organic wastewater treatment[J]. Journal of Environmental Chemical Engineering, 2016, 4(1): 762-787. doi: 10.1016/j.jece.2015.12.016
[13] Li Y, Yang K, Liao X, et al. Quantification of oxidant demand and consumption for in situ chemical oxidation design: In the case of potassium permanganate[J]. Water, Air & Soil Pollution, 2018, 229(11): 375.
[14] Ranc B, Faure P, Croze V, et al. Selection of oxidant doses for in situ chemical oxidation of soils contaminated by polycyclic aromatic hydrocarbons (PAHs): A review[J]. Journal of Hazardous Materials, 2016, 312: 280-297. doi: 10.1016/j.jhazmat.2016.03.068
[15] ASTM. D7262-10. Standard test method for estimating the permanganate natural oxidant demand of soil and aquifer solids[S]. 2010.
[16] Mumford K G, Lamarche C S, Thomson N R. Natural oxidant demand of aquifer materials using the push-pull technique[J]. Journal of Environmental Engineering, 2004, 130(10): 1139-1146. doi: 10.1061/(ASCE)0733-9372(2004)130:10(1139)
[17] Brown R A. In situ chemical oxidation: Performance, practice, and pitfalls. AFCEE Technology Transfer Workshop[R]. San Antonio, 2003.
[18] Liang C, Chien Y C, Lin Y L. Impacts of ISCO persul-fate, peroxide and permanganate oxidants on soils: Soil oxidant demand and soil properties[J]. Soil and Sediment Contamination: An International Journal, 2012, 21(6): 701-719. doi: 10.1080/15320383.2012.691129
[19] Besha A T, Bekele D N, Naidu R, et al. Recent advances in surfactant-enhanced in situ chemical oxidation for the remediation of non-aqueous phase liquid contaminated soils and aquifers[J]. Environmental Technology & Innovation, 2018, 9: 303-322.
[20] Liu J, Liu Z, Zhang F, et al. Thermally activated persulfate oxidation of NAPL chlorinated organic compounds: Effect of soil composition on oxidant demand in different soil-persulfate systems[J]. Water Science and Technology, 2017, 75(8): 1794-1803. doi: 10.2166/wst.2017.052
[21] Huling S G, Pivetz B E. In situ chemical oxidation[R]. EPA, 2006.
[22] Hønning J, Broholm M M, Bjerg P L. Quantification of potassium permanganate consumption and PCE oxidation in subsurface materials[J]. Journal of Contaminant Hydrology, 2007, 90(3-4): 221-239. doi: 10.1016/j.jconhyd.2006.10.002
[23] Liao X, Zhao D, Yan X. Determination of potassium perman-ganate demand variation with depth for oxidation-remediation of soils from a PAHs-contaminated coking plant[J]. Journal of Hazardous Materials, 2011, 193: 164-170. doi: 10.1016/j.jhazmat.2011.07.045
[24] Siegrist R L, Crimi M, Simpkin T J. In situ chemical oxidation for groundwater remediation[M]. Springer Science & Business Media, 2011.
[25] 刘中良, 洪小峰, 舒代容. 有机污染场地氧化剂需求量及不同活化条件下氧化剂降解动力学研究[J]. 环境与发展, 2020, 32(11): 84-86. https://www.cnki.com.cn/Article/CJFDTOTAL-NMHB202011038.htm Liu Z L, Hong X F, Shu D R. Study on oxidant demand and degradation kinetics of oxidant under different activation conditions in organic polluted sites[J]. Environment & Development, 2020, 32(11): 84-86. https://www.cnki.com.cn/Article/CJFDTOTAL-NMHB202011038.htm
[26] Costanza J, Otaño G, Callaghan J, et al. PCE oxidation by sodium persulfate in the presence of solids[J]. Environmental Science & Technology, 2010, 44(24): 9445-9450.
[27] Lee E S, Woo N C, Schwartz F W, et al. Characterization of controlled-release KMnO4 (CRP) barrier system for groundwater remediation: A pilot-scale flow-tank study[J]. Chemosphere, 2008, 71(5): 902-910. doi: 10.1016/j.chemosphere.2007.11.037
[28] Urynowicz M A, Balu B, Udayasankar U. Kinetics of natural oxidant demand by permanganate in aquifer solids[J]. Journal of Contaminant Hydrology, 2008, 96(1-4): 187-194.
[29] Tsitonaki A, Petri B, Crimi M, et al. In situ chemical oxida-tion of contaminated soil and groundwater using persulfate: A review[J]. Critical Reviews in Environmental Science and Technology, 2010, 40(1): 55-91.
[30] Cha K Y, Borden R C. Impact of injection system design on ISCO performance with permanganate-mathematical modeling results[J]. Journal of Contaminant Hydrology, 2012, 128(1): 33-46.
[31] Dangi M B, Urynowicz M A, Udayasankar U. Assessment of the experimental conditions affecting natural oxidant demand of soil by permanganate[J]. Journal of Environmental Chemical Engineering, 2018, 6(4): 5160-5166.
[32] Dangi M B, Urynowicz M A, Schultz C L, et al. A comparison of the soil natural oxidant demand exerted by permanganate, hydrogen peroxide, sodium persulfate, and sodium percarbonate[J]. Environmental Challenges, 2022, 7: 100456.
[33] Yan N, Liu F, Chen Y, et al. Influence of groundwater constituents on 1, 4-dioxane degradation by a binary oxidant system[J]. Water, Air & Soil Pollution, 2016, 227(12): 1-7.
[34] Urynowicz M A. In situ chemical oxidation with perman-ganate: Assessing the competitive interactions between target and nontarget compounds[J]. Soil & Sediment Contamination, 2007, 17(1): 53-62.
[35] Al-Shamsi M A, Thomson N R. Competition by aquifer materials in a bimetallic nanoparticle/persulfate system for the treatment of trichloroethylene[J]. Environmental Science: Processes & Impacts, 2013, 15(10): 1964-1968.
[36] Baciocchi R. Principles, developments and design criteria of in situ chemical oxidation[J]. Water, Air & Soil Pollution, 2013, 224(12): 1-11.
[37] 王文坦, 邵雁, 李社锋, 等. 一种土壤化学需氧量的测定方法: CN201610539931.8[P]. 2016-11-23. Wang W T, Shao Y, Li S F, et al. A method for determination of chemical oxygen demand of soil: CN201610539931.8[P]. 2016-11-23.
[38] 杨勇, 张蒋维, 陈恺, 等. 化学氧化法治理焦化厂PAHs污染土壤[J]. 环境工程学报, 2016, 10(1): 427-431. https://www.cnki.com.cn/Article/CJFDTOTAL-HJJZ201601072.htm Yang Y, Zhang J W, Chen K, et al. Chemical oxidation of coking plant soils contaminated with polycyclic aromatic hydrocarbons[J]. Chinese Journal of Environmental Engineering, 2016, 10(1): 427-431. https://www.cnki.com.cn/Article/CJFDTOTAL-HJJZ201601072.htm
[39] Huang Q, Dong H, Towne R M, et al. Permanganate diffu-sion and reaction in sedimentary rocks[J]. Journal of Contaminant Hydrology, 2014, 159: 36-46.
[40] Xu X, Thomson N R. A long-term bench-scale investi-gation of permanganate consumption by aquifer materials[J]. Journal of Contaminant Hydrology, 2009, 110(3-4): 73-86.
[41] Xu X, Thomson N R. Estimation of the maximum consum-ption of permanganate by aquifer solids using a modified chemical oxygen demand test[J]. Journal of Environmental Engineering, 2008, 134(5): 353-361.
[42] Molnár M. Hydrogen peroxide oxidation for in situ remed-iation of trichloroethylene-from the laboratory to the field[J]. Periodica Polytechnica Chemical Engineering, 2013, 57(1-2): 41-51.
[43] Thomson N, Sra K, Xu X. Improved understanding of in situ chemical oxidation. Technical objective 2: Soil reactivity[R]. 2009.
[44] Xu X. Interaction of chemical oxidants with aquifer materials[D]. Waterloo: University of Waterloo, 2006.
[45] 李旭, 苏世林, 文章, 等. 单井注抽试验测算地下水流速的数值分析[J]. 地球科学, 2022, 47(2): 633-641. https://www.cnki.com.cn/Article/CJFDTOTAL-DQKX202202019.htm Li X, Su S L, Wen Z, et al. Numerical analysis of estimating groundwater velocity through single-well push-pull test[J]. Earth Science, 2022, 47(2): 633-641. https://www.cnki.com.cn/Article/CJFDTOTAL-DQKX202202019.htm
[46] Mathai A. Push-pull tests to support in situ chemical oxidation system design[D]. Waterloo: University of Waterloo, 2012.
[47] 尚晓伟, 姚佳斌, 田文钢, 等. 原位化学氧化技术在有机污染场地中试工程设计研究[J]. 环境与发展, 2020, 32(12): 71-72. https://www.cnki.com.cn/Article/CJFDTOTAL-NMHB202012035.htm Shang X W, Yao J B, Tian W G, et al. Research on pilot project design of in situ chemical oxidation technology in organic contaminated site[J]. Environment and Development, 2020, 32(12): 71-72. https://www.cnki.com.cn/Article/CJFDTOTAL-NMHB202012035.htm
[48] Ko S, Ji S. In situ push-pull tests for the determination of TCE degradation and permanganate consumption rates[J]. Environmental Geology, 2007, 53(2): 359-364.
[49] Hendrych J, Kubal M, Beneš P, et al. The influence of solids characteristics on the specific oxidant consumption by in-situ chemical oxidation using potassium[J]. Acta Montanistica Slovaca, 2008, 13(3): 285-289.
[50] Bendouz M, Dionne J, Tran L H, et al. Polycyclic aromatic hydrocarbon oxidation from concentrates issued from an attrition process of polluted soil using the Fenton reagent and permanganate[J]. Water, Air & Soil Pollution, 2017, 228(3): 115.
[51] Teel A L, Elloy F C, Watts R J. Persulfate activation during exertion of total oxidant demand[J]. Chemosphere, 2016, 158: 184-192.
[52] Xu X, Thomson N R. Hydrogen peroxide persistence in the presence of aquifer materials[J]. Soil & Sediment Contamination, 2010, 19(5): 602-616.
-
期刊类型引用(1)
1. 王聪聪,陈家玮. 铁基生物炭活化过硫酸盐非自由基途径主导高效降解诺氟沙星. 水文地质工程地质. 2024(02): 66-76 .  百度学术
百度学术
其他类型引用(1)
计量
- 文章访问数: 140
- HTML全文浏览量: 73
- PDF下载量: 29
- 被引次数: 2



 下载:
下载:
 京公网安备 11010202008159号
京公网安备 11010202008159号