Determination of the Redox Potential for Aqueous Fe(Ⅱ)-Goethite Heterogeneous Systems by Potentiometric Method
-
摘要:
溶解性二价铁(Feaq 2+)-铁氧化物非均相体系的氧化还原能力显著影响含水层中有毒重金属和有机污染物的迁移转化行为。然而,非均相体系氧化还原电位(Eh)的测定存在平衡缓慢和结果不稳定等难题,故亟待开发与优化电化学法快速准确测定Eh,实现Feaq 2+-铁氧化物非均相体系氧化还原能力的定量表征。本文选取针铁矿作为常见的铁氧化物,探讨了介导和非介导电位法测定Feaq 2+-针铁矿非均相体系Eh的优化实验条件,研究了介导物质的类型与添加顺序以及工作电极预处理方法等条件对Eh测定的影响,并通过能斯特方程验证电位法的可行性。结果表明:工作电极的表面状态、介导物质的选择以及针铁矿-工作电极之间平衡的建立对Eh 测定十分关键。介导法能有效地缩短测定时间,但需要选择合适的介导物质;非介导法需确保工作电极与针铁矿之间平衡的建立。同时,利用非介导法测定了不同pH和Feaq 2+浓度下不同粒径针铁矿与Feaq 2+非均相体系的Eh,根据能斯特方程和最小二乘法多元线性拟合得到不同粒径针铁矿的标准氧化还原电位(Eh0),对于粒径为200、700和1000nm的针铁矿Eh0分别为815、802和782mV,验证了优化后电位法的可行性。本文的结论可为矿物非均相体系Eh的测定提供方法学参考,也为预测Feaq 2+-铁氧化物非均相体系参与的污染物衰减速率提供理论支撑。
Abstract:The redox properties of Feaq 2+-iron oxide heterogeneous systems play an important role in the environmental behaviors of heavy metal and organic pollutants. However, the determination of Eh for heterogeneous systems is still challenging due to the redox equilibration between the electrode and suspension is sluggish. In this study, goethite was chosen as the representative of iron oxide in the aquifer. Both mediated and non-mediated potential methods were conducted to obtain the Eh of Feaq 2+-goethite heterogeneous system through the optimizing of measurement conditions. Moreover, the effect of the working electrode surface state, the kind of mediators, and the equilibrium time on the Eh measurement were investigated. The results indicated that the working electrode surface state, the suitable mediators, and the establishment of equilibrium were crucial for obtaining accurate Eh. Compared with the non-mediated potentiometric method, the mediated method can shorten the determination time, but the appropriate mediator must be chosen. In non-mediated potentiometric method, the equilibrium between the working electrode and goethite must be established. The standard redox potential (Eh0) of goethite with different particle sizes was obtained, which demonstrated the practicability of this method. The results provide the method for the Eh measurement of mineral heterogeneous systems, and also provide theoretical support for predicting the pollutant abiotic attenuation rate induced by Feaq 2+-iron oxide heterogeneous systems.
-
Keywords:
- dissolved bivalent iron /
- iron oxide /
- heterogeneous system /
- redox potential /
- goethite
-
X射线荧光光谱定性分析技术经过长期的应用及发展,其应用范围也越来越广泛[1-4]。目前,XRF所带的定性分析软件(SQX)可自动对扫描谱图进行搜索和匹配,包括确定峰位、背景和峰位的净强度[5-7],并从XRF特征谱线数据库中配对确定元素的谱线,这对从事XRF的分析者而言非常便利[8-10]。近年来刘岩等[11]采用XRF无标样分析法检测催化剂,测定结果的相对标准偏差小于1.3%;张红菊等[12]采用XRF无标样分析法检测轻合金铝合金中的主量元素,其测量值与认定值的相对误差低于±5%,测量结果都具有很好的可靠性和准确度。
自然界矿物种类复杂,应用XRF半定量分析软件(SQX)分析未知样品时,由于SQX软件仅对样品中9F~92U元素进行半定量分析,而对H2O、C这些参数不能直接测定。对于烧失量(LOI)、结晶水(H2O+)含量较高的铝土矿,二氧化碳含量较高的碳酸盐矿物,硫、碳含量较高的硫化物金属矿这类高烧失量矿物样品,平衡归一化计算时对未知样品中的Al2O3、SiO2、CaO、MgO、Fe等主要元素分析结果影响较大,半定量分析数据准确度较低。这就要求XRF分析人员需要掌握未知样品的来源及基本情况,根据测定结果对各元素在样品中的结构状态进行评估,选用更为合理的校正模式,提高半定量分析的准确性[13-15]。为了解决这个问题,本文提出了一种校正模式。该校正模式根据半定量分析初步结果,采用重量法、碘量法、酸碱测定法、红外光谱法有选择性地对未知样品中的LOI、S、C、H2O+等项目进行定量分析,然后将定量分析结果输入SQX该参数的固定结果中,二次平衡归一计算得出新的半定量分析结果。应用该校正模式校正后,铝土矿、碳酸盐矿物、硫化物金属矿等高烧失量矿物的半定量分析结果的准确度得到大幅度提高。
1. 实验部分
1.1 仪器与测量条件
ZSX PrimusⅣ型顺序扫描波长色散X射线荧光光谱仪(日本理学电机工业株式会社),端窗铑靶X射线管,工作电压20~60kV,工作电流2~160mA,铍窗厚度30μm,视野光栏0.5~30mm,准直器: S2/S4,探测器: PC/SC,分光晶体:RX 25/Ge/PET/LiF200[16-19]。测量元素范围9F~92U。BP-1型压样机(丹东北方科学仪器公司)。各元素具体的测量条件见表 1。
表 1 仪器测量条件Table 1. Measuring conditions of the XRF equipment分析元素 数据库 靶材 电流
(kV)电压
(mA)滤光片 衰减器 准直器 晶体 探测器 PHA 重元素 Standard Rh 50 60 OUT 1/1 S2 LiF(200) SC 100~300 重元素(1) Sta-Ni400 Rh 50 60 Ni-400 1/1 S2 LiF(200) SC 150~250 Ca-Kα Standard Rh 40 75 OUT 1/1 S4 LiF(200) PC 100~300 K-Kα Standard Rh 40 75 OUT 1/1 S2 LiF(200) PC 100~300 Cl-Kα Standard Rh 30 100 OUT 1/1 S4 Ge PC 150~300 S-Kα Standard Rh 30 100 OUT 1/1 S4 Ge PC 150~300 P-Kα Standard Rh 30 100 OUT 1/1 S4 Ge PC 150~300 Si-Kα Standard Rh 30 100 OUT 1/1 S4 PET PC 100~300 Al-Kα Standard Rh 30 100 OUT 1/1 S4 PET PC 100~250 Mg-Kα Standard Rh 30 100 OUT 1/1 S4 RX25 PC 100~250 Na-Kα Standard Rh 30 100 OUT 1/1 S4 RX25 PC 100~250 F-Kα Standard Rh 40 75 OUT 1/1 S4 RX25 PC 100~300 1.2 SQX分析模拟计算流程
XRF半定量分析可选择测定未知样品中F~U或Ti~U之间的元素,分析测试程序完成后会自动报出大于仪检出限的各元素的分析结果,这时应根据测试结果作一个初步判断是否需要进行SQX计算;如不需要,则可以直接报出测定结果;如测定结果与样品实际结构状态有较大差别,则需选用更为合适的校正模式、平衡组分或添加其他方法测试结果后进行SQX计算,以得到更为合理的测定结果。定性分析的基本流程见图 1。
1.3 样品制备及实验方法
为验证本文提出的半定量分析模式分析校正效果,选用国家标准物质铝土矿GBW(E)70036、碳酸盐矿物GBW07131、硫化物多金属矿GBW07166作为待测样品,在105℃下烘干2h,称取4.5±0.1g,倒入放置于平板模具上的PVC塑料环(外径40mm,内径35mm,高5mm)中,在30t压力下加压30s压制成型,编号,置于样品盒内,用X射线荧光光谱仪半定量分析方法进行测试[20-22]。仪器自动计算出各元素的含量。
根据XRF半定量初步分析结果,按化学标准方法YS/T 575.19—2007、GB/T 3286.8—2014、GB/T 3286.7—2014、GB/T 14353.12—2010、GB/T 8151.2—2012、SN/T 3598—2013、GB/T 2469—1996、YS/T 575.18—2007选择性分析未知样品中的烧失量(LOI)、硫(S)、碳(C)、结晶水(H2O+),计算出定量结果,备用。
将化学分析结果作为XRF半定量分析软件(SQX)中该元素的固定结果,重新进行平衡计算出新的半定量结果。
2. 结果与讨论
2.1 烧失量对铝土矿类型矿物半定量分析结果的影响
铝土矿是一种土状矿物,化学组成为Al2O3·nH2O,含水不定,多为单水或三水矿物[23-24]。由于XRF的局限性,对于H2O、C这些未定量的参数,其含量在铝土矿中较高[25],平衡归一化计算时会对Al2O3、SiO2、Fe2O3等元素的影响较大。这时可采用烧失量校正的方法,添加烧失量(LOI)作为该样品的固定值,运行半定量分析软件(SQX)重新计算出新的结果。将GBW(E)70036作为未知样品用XRF定性分析方法进行分析,各种校正模式的计算值与认定值对照结果见表 2。
表 2 铝土矿标准物质GBW(E)70036各种校正模式计算值与认定值对比Table 2. Calculated values and standard values of bauxite standard material GBW(E)70036 in various correction models分析元素 氧化物模式测试
结果(%)添加LOI校正结果
(%)H2O作平衡
校正结果(%)GBW(E)70036
认定值(%)氧化物模式测试结果
相对误差(%)LOI校正结果
相对误差(%)MgO 0.136 0.121 0.116 0.120 13.33 0.83 Al2O3 76.94 67.51 64.46 69.74 10.32 -3.20 SiO2 7.91 6.62 6.12 4.88 62.09 35.66 P2O5 0.159 0.132 0.121 0.120 32.50 10.00 SO3 0.182 0.00 0.139 0.047 - - K2O 1.07 0.880 0.810 0.710 50.70 23.94 CaO 0.258 0.212 0.195 0.180 43.33 17.78 TiO2 5.10 4.17 3.81 3.97 28.46 5.04 Fe2O3 7.42 5.97 5.35 6.09 21.84 -1.97 LOI * 13.70 △ 13.74 - - H2O * △ 18.26 - - - 注:“*”表示XRF不能直接分析该参数,无数据;“△”表示在LOI或H2O其中一项参数有测量结果时,另一项结果不参与校正计算;“-”表示未定值或未统计计算。 据表 2可知,GBW(E)70036以氧化物模式的测试结果与认定值误差较大,当添加LOI校正计算后,其多个元素的平均相对误差由32.8%降至12.3%,准确度大幅提高。此外,在确定未知样品是未经高温灼烧的情况下,还可以采用H2O作为平衡组分直接计算,其计算结果也与认定值较为相近。
2.2 二氧化碳与烧失量对碳酸盐类型矿物半定量分析结果的影响
碳酸盐矿物中CO2的占比较高, 而CO2是SQX软件未能定量参数之一,给定性分析结果带来较大误差。为提高定性分析的准确度,可对CO2或烧失量进行定量分析[26],添加烧失量或CO2定量分析结果作为该样品的固定值,运行SQX重新计算出新的结果。将GBW07131作为未知样品用XRF定性分析方法进行分析,各种校正模式的计算值与认定值对照结果见表 3。
表 3 碳酸盐标准物质GBW07131各种校正模式计算值与认定值对比Table 3. Calculated values and standard values of carbonate standard material GBW07131 in various correction models分析元素 氧化物模式
测试结果(%)CO2平衡
校正结果(%)添加LOI
校正结果(%)钙镁元素以碳酸盐
计平衡计算(%)GBW07131
认定值(%)氧化物模式测试
结果相对误差(%)LOI校正结果
相对误差(%)MgO 29.73 19.57 19.18 20.4 20.14 47.62 4.77 Al2O3 0.759 0.454 0.449 0.451 0.290 161.72 -54.83 SiO2 2.18 1.29 1.27 1.28 1.15 89.57 -10.43 P2O5 0.051 0.030 0.030 0.030 0.016 218.75 -87.50 SO3 0.442 0.256 0.00 0.254 - - - K2O 0.292 0.161 0.160 0.160 0.160 82.50 0.00 CaO 64.54 31.76 32.07 31.50 30.93 108.66 -3.69 TiO2 0.045 0.018 0.0186 0.0178 0.013 246.15 -43.08 MnO 0.038 0.015 0.016 0.011 0.012 216.67 -33.33 Fe2O3 0.435 0.169 0.176 0.167 0.170 155.88 -3.53 CO2 * 45.66 △ - - - - LOI * △ 45.67 - 45.73 - 0.13 注:“*”表示XRF不能直接分析该参数,无数据;“△”表示在LOI或CO2其中一项参数有测量结果时,另一项结果不参与校正计算;“-”表示未定值或未统计计算。 据表 3可知,GBW07131以氧化物模式测试结果较认定值误差较大。当添加LOI校正计算后,其多个元素的平均相对误差由122.4%降至27.2%,准确度大幅提高。此外,采用滴加稀盐酸确定未知样品是碳酸盐矿物的情况下,可以采用CO2作为平衡组分直接计算或者将CaO、MgO换算成为CaCO3、MgCO3计算模式重新平衡计算,其结果也与认定值较为相近。
2.3 碳硫元素对硫化物多金属矿类型矿物半定量分析结果的影响
硫化物多金属矿中的碳、硫元素含量较高,以氧化物模式对该类型样品进行半定量分析时误差较大。当采用化学法测定这类样品的烧失量时,硫化物金属矿中的硫在高温下会被空气中的氧替换,不仅会出现烧蚀减量,还会出现烧蚀增量,使得烧失量的结果是不准确的[27-28],因此不能把烧失量校作为该未知样品的固定值对测定结果进行平衡计算。这时可以采用化学法测定该未知样品中的C、S元素,作为该样品的固定值,运行半定量分析软件(SQX)重新计算出新的结果。将GBW07166作为未知样品用XRF半定量程序进行分析,各种校正模式的计算值与认定值对照结果见表 4。
表 4 硫化矿多金属矿标准物质GBW07166各种校正模式计算值与认定值对比Table 4. Calculated values and standard values of sulfide polymetallic ore standard material GBW07166 in various correction models分析元素 氧化物模式测试
结果(%)总硫、总碳固定
平衡计算(%)LOI平衡计算
(%)Sulfide模式
校正结果(%)GBW07166
认定值(%)氧化物模式测试
结果相对误差(%)总硫、总碳校正
结果相对误差(%)MgO 0.360 0.350 0.675 0.505 0.310 16.13 12.90 Al2O3 1.60 1.55 3.03 2.29 1.25 28.00 24.00 SiO2 3.34 3.50 6.26 4.86 3.78 -11.64 7.41 S 18.43 33.80 0.00 27.75 33.80 - - K2O 0.306 0.433 0.387 0.484 0.320 -4.38 35.31 CaO 2.05 2.02 2.61 3.27 1.96 4.59 3.06 Fe 18.22 28.58 27.45 30.84 29.60 -38.45 -3.45 Cu 15.50 28.00 30.72 28.42 24.20 -35.95 15.70 Zn 0.025 0.057 0.049 0.055 0.057 -56.14 0.00 C * 0.138 △ - - - - LOI * △ 27.04 - - - - 注:“*”表示XRF不能直接分析该参数,无数据;“△”表示在LOI或C其中一项参数有测量结果时,另一项结果不参与校正计算;“-”表示未定值或未统计计算。 据表 4可知,GBW07166以氧化物模式或添加LOI校正计算结果后,测试结果较认定值误差较大,当添加全硫、全碳校正计算结果后,其多个元素的平均相对误差由27.2%降至9.5%,准确度大幅提高。此外,在没有条件测定全硫、全碳元素时,选用SQX软件中Sulfide校正模式重新平衡计算,其结果也与认定值较为相近。
3. 应用实例
选取3件不同类型的未知样品,应用XRF半定量程序分析,根据XRF半定量初步分析结果,计算对照结果见表 5。未知样品1、2在添加烧失量(LOI)校正计算后半定量分析结果与化学法分析结果比较,多个元素的平均相对误差分别由46.2%降至18.0%和37.6%降至7.1%。未知样品3添加总硫、总碳校正计算结果后,其多个元素的平均相对误差由28.1%降至10%,准确度得到了明显提高。若与DZ/T 130—2006《地质矿产实验室测试质量管理规范》要求定量分析规范中误差允许限(Yc)相比较,除少部分项目能满足规范要求外,大部分项目还是达不到定量分析要求。但是如铝土矿中的Al2O3,碳酸盐矿物中的CaO、MgO,硫化物多金属矿中Fe、Zn、Cu、Pb等元素的相对误差均在5%以内,与DZ/T 130—2006要求较为接近。
表 5 某未知样品各种校正模式的计算值与化学分析值对比Table 5. Calculated values and chemical analysis values of various correction modes for the unknown sample样品编号 分析元素 氧化物模式测试
结果(%)平衡校准计算
结果(%)化学法测定值
(%)氧化物模式测试
结果相对误差(%)平衡校准计算结果
相对误差(%)允许限Yc
(%)Al2O3 86.97 76.11 78.01 11.49 -2.44 0.63 SiO2 2.94 1.82 1.31 124.43 38.93 4.17 Fe2O3 3.26 2.54 2.55 24.84 -0.46 5.11 TiO2 4.29 3.4 3.10 38.38 9.78 4.80 未知样品1 K2O 0.19 0.17 0.16 18.75 6.25 10.45 CaO 0.33 0.31 0.31 6.45 0.00 9.00 MgO 0.29 0.25 0.20 45.00 25.00 9.95 P2O5 0.28 0.22 0.14 100.00 61.37 10.76 LOI * 14.6 14.6 - - 2.58 Na2O 0.76 0.71 0.781 -2.59 -8.72 7.17 MgO 0.29 0.24 0.21 39.14 14.95 9.84 Al2O3 0.48 0.39 0.31 54.13 26.16 9.00 SiO2 1.15 0.93 0.83 38.66 12.45 7.05 P2O5 1.24 1.00 0.97 28.34 2.88 6.77 Fe2O3 1.70 1.21 1.18 44.18 2.13 6.41 未知样品2 S 4.72 △ 3.21 47.04 - 4.74 CaO 1.13 0.81 0.83 36.64 -2.40 7.05 Cr 18.49 13.09 12.89 43.46 1.53 2.75 Ni 22.81 16.18 16 42.55 1.12 2.47 Cu 14.53 10.31 10.33 40.62 -0.23 3.04 Zn 3.04 2.16 2.02 43.24 5.94 5.49 LOI * 37.00 37.00 - - - MgO 0.21 0.200 0.185 14.49 8.11 10.12 Al2O3 0.53 0.472 0.427 23.87 10.61 8.34 SiO2 2.18 1.818 1.650 32.00 10.15 5.83 P2O5 0.02 0.024 0.028 -34.29 -13.21 14.91 S 18.84 34.02 34.02 - - - K2O 0.05 0.048 0.042 15.44 13.31 13.77 未知样品3 CaO 0.15 0.127 0.137 7.72 -7.50 10.81 TiO2 0.03 0.031 0.026 30.98 20.78 15.18 Fe 4.52 6.942 6.720 -32.81 3.31 3.64 Cu 0.68 1.057 1.218 -44.37 -13.18 6.36 Zn 32.24 50.517 48.250 -33.18 4.70 1.15 Pb 1.58 2.505 2.646 -40.46 -5.33 5.05 C * 1.21 1.21 - - - 注:“*”表示XRF不能直接分析该参数,无数据;“△”表示在LOI有测量结果时,该项结果不参与校正计算;“-”表示未定值或未统计计算。 4. 结论
实验证明采用本文提出的校正模式进行校正,分析铝土矿、碳酸盐矿物和硫化物多金属矿中多元素的平均准确度提高了2.6~4.5倍,半定量分析结果准确度大幅提高。其中,铝土矿中的Al2O3,碳酸盐矿物中的CaO、MgO,硫化物矿物中Fe、Zn、Cu、Pb等主量元素的相对误差均在5%以内,与化学法分析结果较为相近。本方法可快速、较为准确地测定铝土矿、碳酸盐矿物和硫化物矿物中多元素的含量。
这种化学法与半定量分析软件相结合的半定量校正模式,不仅可用于铝土矿、碳酸盐矿物和硫化物矿物,还适用于烧失量较高的锰矿、磷矿等矿物的压片半定量分析[29-30]。对于硫化物矿物等多金属矿的定量全分析,因为这类矿物容易腐蚀铂坩埚而很少采用熔片制样XRF分析[31],通常采用化学分析法,但流程繁琐,本文研究方法可作为一种有效的矿石全分析的补充手段。
-
图 1 介导电位法中不同介导物质测定Feaq 2+-针铁矿非均相体系的Eh(a);不同介导物质循环伏安曲线(b);介导物质CMV(c)和AQS(d)添加时间对Feaq 2+-针铁矿非均相体系Eh测定的影响
Figure 1. Determination of Eh in Feaq 2+-goethite heterogeneous system using different mediating substances in the mediated potentiometry (a); Cyclic voltammetry curves of different mediated substances (b); The effect of adding time of mediated substance CMV (c) and AQS (d) on the determination of Eh in Feaq 2+-goethite heterogeneous system.
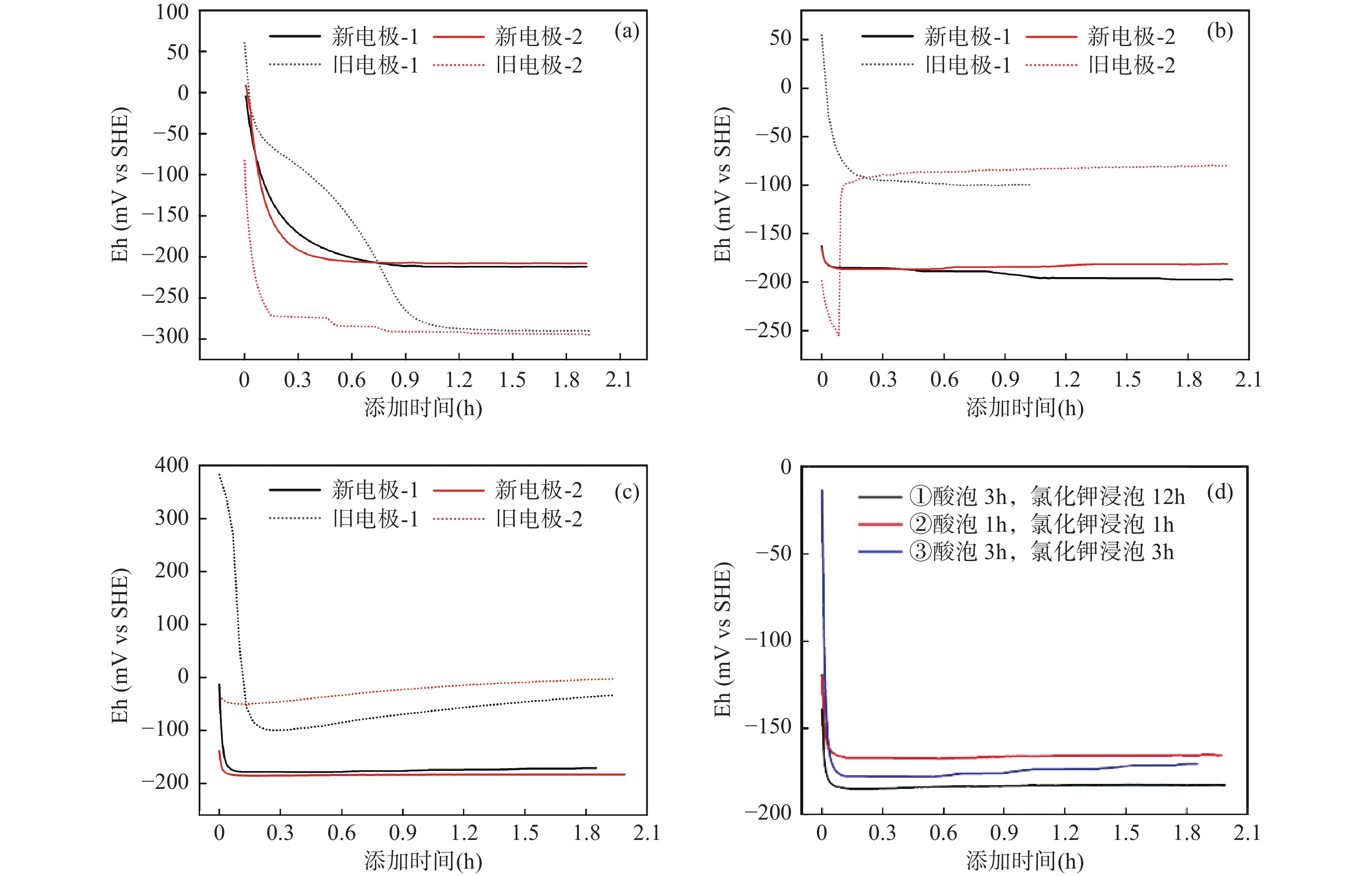
图 3 电极钝化及电极预处理时间对电位法测定Fe2+-针铁矿非均相体系Eh的影响:(a)不加介导物质;(b)加入 CMV; (c)加入 AQS;(d)电极预处理时间对介导电位法测定Fe2+-针铁矿非均相体系Eh的影响(AQS为介导物质)
Figure 3. The effect of electrode passivation and electrode pretreatment time on the determination of Eh in Feaq 2+-goethite heterogeneous system by potentiometric methods: (a) Without the addition of mediator; (b) Addition of CMV; (c) Addition of AQS; (d) The effect of electrode pretreatment time on the determination of Eh in Feaq 2+-goethite heterogeneous system using mediated potentiometry (AQS as the mediator)
表 1 不同pH和Feaq 2+浓度下应用介导电位法与非介导电位法测定Eh的对比
Table 1 Comparison of Eh values obtained by mediated and non-mediated potentiometric method under different pH and Feaq 2+ concentrations
实验条件 非介导法
Eh测定值
(mV)介导法Eh测定值
(mV)Eh理论值
(Eh0=804mV)差异(mV) Ru CMV AQS 非介导法 Ru CMV AQS Feaq 2+ 0.75mmol/L,pH 6 −90 +21 / / −56 −34 77 / / Feaq 2+ 0.38mmol/L,pH 7 −211 / −176 −185 −215 +4 / +39 +30 注:“/”表示未取得实验测定值。 -
[1] 郭华明, 高志鹏, 修伟. 地下水典型氧化还原敏感组分迁移转化的研究热点和趋势[J]. 地学前缘, 2022, 29(3): 64−75. doi: 10.13745/j.esf.sf.2022.1.37 Guo H M, Gao Z P, Xiu W. Typical redox-sensitive components in groundwater systems: Research highlights and trends[J]. Earth Science Frontiers, 2022, 29(3): 64−75. doi: 10.13745/j.esf.sf.2022.1.37
[2] Kappler A, Bryce C, Mansor M, et al. An evolving view on biogeochemical cycling of iron[J]. Nature Reviews Microbiology, 2021, 19(6): 360−374. doi: 10.1038/s41579-020-00502-7
[3] Coyte R M, Vengosh A. Factors controlling the risks of co-occurrence of the redox-sensitive elements of arsenic, chromium, vanadium, and uranium in groundwater from the Eastern United States[J]. Environmental Science & Technology, 2020, 54(7): 4367−4375. doi: 10.1021/acs.est.9b06471
[4] Borch T, Campbell K, Kretzschmar R, et al. How electron flow controls contaminant dynamics[J]. Environmental Science & Technology, 2010, 44(1): 3−6. doi: 10.1021/es903264z
[5] 姚远, 余光辉, 滕辉. 土壤铁氧化物-亚铁的相互作用及其环境影响研究进展[J]. 土壤, 2023, 55(4): 718−728. doi: 10.13758/j.cnki.tr.2023.04.004 Yao Y, Yu G H, Teng H. Soil iron oxide-ferrous interaction and its environmental effects: A review[J]. Soils, 2023, 55(4): 718−728. doi: 10.13758/j.cnki.tr.2023.04.004
[6] 胡敏, 李芳柏, 土壤微生物铁循环及其环境意义[J]. 土壤学报, 2014, 51(4): 683−698. Hu M, Li F B. Soil microbe mediated iron cycling and its environmental implication[J]. Acta Pedologica Sinica, 2014, 51(4): 683−698.
[7] Kappler A, Schink B, Newman D K. Fe(Ⅲ) mineral formation and cell encrustation by the nitrate-dependent Fe(Ⅱ)-oxidizer strain bofen1[J]. Geobiology, 2005, 3(4): 235−245. doi: 10.1111/j.1472-4669.2006.00056.x
[8] 罗伟嘉, 冯晨, 侯国华, 等. 铁氧化物-二价铁体系在潜流带低渗透区的氧化还原特性研究进展[J]. 岩矿测试, 2024, 43(2): 375−396. doi: 10.15898/j.ykcs.202309090150 Luo W J, Feng C, Hou G H, et al. Progress on redox characteristics of an iron oxide-ferrous system in the hyporheic zone[J]. Rock and Mineral Analysis, 2024, 43(2): 375−396. doi: 10.15898/j.ykcs.202309090150
[9] 谷春云, 廖高明, 邓一荣, 等. FeS介导下的1, 2-二溴乙烷非生物自然衰减[J]. 中国环境科学, 2023, 43(9): 4632−4638. doi: 10.19674/j.cnki.issn1000-6923.20230523.009 Gu C Y, Liao G M, Deng Y R, et al. The abiotic natural attenuation of 1, 2-dibromoethane mediated by FeS[J]. China Environmental Science, 2023, 43(9): 4632−4638. doi: 10.19674/j.cnki.issn1000-6923.20230523.009
[10] 廖高明, 马杰, 谷春云, 等. 污染场地卤代烃非生物自然衰减研究进展[J]. 环境科学研究, 2021, 34(3): 742−754. doi: 10.13198/j.issn.1001-6929.2020.09.14 Liao G M, Ma J, Gu C Y, et al. Research progress on abiotic natural attenuation of halogenated hydrocarbons at contaminated sites[J]. Research of Environmental Sciences, 2021, 34(3): 742−754. doi: 10.13198/j.issn.1001-6929.2020.09.14
[11] Cardenas-Hernandez P A, Anderson K A, Murillo-Gelvez J, et al. Reduction of 3-nitro-1, 2, 4-triazol-5-one (NTO) by the hematite-aqueous Fe(Ⅱ) redox couple[J]. Environmental Science & Technology, 2020, 54(19): 12191−12201. doi: 10.1021/acs.est.0c03872
[12] 王娜, 王家松, 曾江萍, 等. 重铬酸钾和高锰酸钾电位落差法测定砂岩型铀矿氧化还原电位的探讨[J]. 岩矿测试, 2022, 41(5): 806−814. doi: 10.15898/j.cnki.11-2131/td.202112080199 Wang N, Wang J S, Zeng J P, et al. Determination of redox potential of sandstone-type uranium ore by potential drop methods of potassium dichromate and potassium permanganate[J]. Rock and Mineral Analysis, 2022, 41(5): 806−814. doi: 10.15898/j.cnki.11-2131/td.202112080199
[13] Neumann A, Hofstetter T B, Luessi M, et al. Assessing the redox reactivity of structural iron in smectites using nitroaromatic compounds as kinetic probes[J]. Environmental Science & Technology, 2008, 42(22): 8381−8387. doi: 10.1021/es801840x
[14] Aeschbacher M, Sander M, Schwarzenbach R P. Novel electrochemical approach to assess the redox properties of humic substances[J]. Environmental Science & Technology, 2010, 44(1): 87−93. doi: 10.1021/es902627p
[15] Sander M, Hofstetter T B, Gorski C A. Electrochemical analyses of redox-active iron minerals: A review of nonmediated and mediated approaches[J]. Environmental Science & Technology, 2015, 49(10): 5862−5878. doi: 10.1021/acs.est.5b00006
[16] Aeppli M, Kaegi R, Kretzschmar R, et al. Electrochemical analysis of changes in iron oxide reducibility during abiotic ferrihydrite transformation into goethite and magnetite[J]. Environmental Science & Technology, 2019, 53(7): 3568−3578. doi: 10.1021/acs.est.8b07190
[17] 陈袁波, 邓思宇, 余珂, 等. 泥炭沼泽湿地土壤分解过程中可溶性有机质氧化还原能力变化特征及其影响机制[J]. 生态学报, 2020, 40(24): 8948−8957. Chen Y B, Deng S Y, Yu K, et al. Change and influence mechanism of the dissolved organic matter redox capacity during peat bog soil decomposition[J]. Acta Ecologica Sinica, 2020, 40(24): 8948−8957.
[18] Kocur C M D, Fan D, Tratnyek P G, et al. Predicting abiotic reduction rates using cryogenically collected soil cores and mediated reduction potential measurements[J]. Environmental Science & Technology Letters, 2019, 7(1): 20−26. doi: 10.1021/acs.estlett.9b00665
[19] Gorski C A, Edwards R, Sander M, et al. Thermo-dynamic characterization of iron oxide-aqueous Fe2+ redox couples[J]. Environmental Science & Technology, 2016, 50(16): 8538−8547. doi: 10.1021/acs.est.6b02661
[20] Shi Z, Nurmi J T, Tratnyek P G. Effects of nano zero-valent iron on oxidation-reduction potential[J]. Environmental Science & Technology, 2011, 45(4): 1586−1592. doi: 10.1021/es103185t
[21] Aeppli M, Voegelin A, Gorski C A, et al. Mediated electrochemical reduction of iron (oxyhydr-) oxides under defined thermodynamic boundary conditions[J]. Environmental Science & Technology, 2018, 52(2): 560−570. doi: 10.1021/acs.est.7b04411
[22] 李欣, 杨珊珊, 刘菲, 等. 典型铁氧化物-Fe(Ⅱ)aq非均相体系氧化还原电位的测定方法[J]. 分析化学, 2023, 51(12): 1935−1944. doi: 10.19756/j.issn.0253-3820.231037 Li X, Yang S S, Liu F, et al. Detection of redox potential of typical iron oxide-Fe(Ⅱ)aq heterogeneous system[J]. Chinese Journal of Analytical Chemistry, 2023, 51(12): 1935−1944. doi: 10.19756/j.issn.0253-3820.231037
[23] Robinson T C, Latta D E, Leddy J, et al. Redox potentials of magnetite suspensions under reducing conditions[J]. Environmental Science & Technology, 2022, 56(23): 17454−17461. doi: 10.1021/acs.est.2c05196
[24] Wang D, Crowe W E, Strongin R M, et al. Exploring the pH dependence of viologen reduction by α-carbon radicals derived from Hcy and Cys[J]. Chemical Communications, 2009(14): 1876−1878. doi: 10.1039/b819746f
[25] Villacis-Garcia M, Ugalde-Arzate M, Vaca-Escobar K, et al. Laboratory synthesis of goethite and ferrihydrite of controlled particle sizes[J]. Boletin De La Sociedad Geologica Mexicana, 2015, 67(3): 433−446. doi: 10.18268/BSGM2015v67n3a7
[26] Tamura H, Goto K, Yotsuyanagi T, et al. Spectrophotometric determination of iron(Ⅱ) with 1, 10-phenanthroline in the presence of large amounts of iron(Ⅲ)[J]. Talanta, 1974, 21(4): 314−318. doi: 10.1016/0039-9140(74)80012-3
[27] Fultz M L, Durst R A. Mediator compounds for the electrochemical study of biological redox systems a compilation[J]. Analytica Chimica Acta, 1982, 140(1): 1−18. doi: 10.1016/s0003-2670(01)95447-9
[28] Roden E E. Geochemical and microbiological controls on dissimilatory iron reduction[J]. Comptes Rendus Geoscience, 2006, 338(6−7): 456−467. doi: 10.1016/j.crte.2006.04.009
[29] Teasdale P R, Minett A I, Dixon K, et al. Practical improvements for redox potential (Eh) measurements and the application of a multiple-electrode redox probe (MERP) for characterizing sediment in situ[J]. Analytica Chimica Acta, 1998, 367(1-3): 201−213. doi: 10.1016/s0003-2670(98)00171-8
[30] Chen G, Thompson A, Gorski C A. Disentangling the size-dependent redox reactivity of iron oxides using thermodynamic relationships[J]. Proceedings of the National Academy of Sciences, 2022, 119(40): 1−10. doi: 10.1073/pnas.2204673119
[31] Stewart S M, Hofstetter T B, Joshi P, et al. Linking thermodynamics to pollutant reduction kinetics by Fe2+ bound to iron oxides[J]. Environmental Science & Technology, 2018, 52(10): 5600−5609. doi: 10.1021/acs.est.8b00481
-
期刊类型引用(5)
1. 刘畅,胡骏翔,苑芷茜. 应用PXRF与ICP-OES法测定土壤中锰的比对研究. 环境科学与管理. 2023(07): 115-119 .  百度学术
百度学术
2. 田戈,刘卫,郭颖超,马春红,张文宇,谷周雷. 恒温振荡浸提-电感耦合等离子体发射光谱法测定土壤中的交换性锰. 中国土壤与肥料. 2023(08): 243-248 .  百度学术
百度学术
3. 杨晓红,陈丽琼,刘婉秋. X射线荧光光谱法在环境监测中的发展与应用. 理化检验-化学分册. 2022(07): 861-868 .  百度学术
百度学术
4. 徐冬梅,陈晋,张敏. WDXRF法测定污染土壤和沉积物中金属元素. 环境监测管理与技术. 2022(06): 52-55+68 .  百度学术
百度学术
5. 刘宏,付淑惠,李海霞,靳晧琛,余恒. X射线荧光光谱仪滤光片故障解决思路探讨. 四川环境. 2022(06): 254-259 .  百度学术
百度学术
其他类型引用(2)



 下载:
下载:





 京公网安备 11010202008159号
京公网安备 11010202008159号