Determination of Hydrolysable Nitrogen in Soil Samples by Alkaline Hydrolysis Diffusion Separation Acid-base Titration Based on a Polypropylene Diffusion Dish
-
摘要:
传统的碱解扩散分离-酸碱滴定法测定土壤样品中的水解性氮,通常采用玻璃扩散皿进行碱解扩散分离。但是使用该法对样品进行前处理和碱解扩散分离过程中,操作者常会面临如下三种困扰:一是玻璃扩散皿内室溶液极易被氢氧化钠溶液和碱性胶液污染;二是玻璃扩散皿和盖子之间容易出现氨气泄漏,而且发现时往往无法解决;三是玻璃扩散皿比较笨重易碎,实验操作不方便;最终导致测定结果不稳定性和操作者对该法体验不佳。本文采用聚丙烯扩散皿,通过改进扩散皿清洗方法和提升扩散皿密封性、统一还原剂加入量和氢氧化钠溶液浓度(1.8mol/L)、适当增加氢氧化钠溶液的加入体积和降低盐酸标准溶液浓度,提高了水解性氮测定的稳定性和准确性。该方法中发生的污染明显降低,避免了发生氨气泄漏,操作便捷。应用于分析土壤有效态标准物质的测定值与标准值一致,如水解性氮测定值< 50mg/kg的标准物质GBW07416a,其绝对偏差为0.2~1.8mg/kg;水解性氮测定值在50~200mg/kg的标准物质GBW07415a、NSA-1、NSA-4、NSA-5、NSA-6,其绝对偏差为0~4.0mg/kg。还原剂对硝态氮转化为铵态氮的加标回收率在89.6%~96.4%之间。该方法可满足测定土壤样品中水解性氮含量的要求。
要点(1) 比较了玻璃和聚丙烯扩散皿的各自特点以及对土壤水解性氮测定结果的影响。
(2) 使用聚丙烯扩散皿并改进器皿清洗方法、提升密封性能,提高了水解性氮测定的稳定性和实验操作的便捷性。
(3) 测定土壤样品中水解性氮,都应加还原剂,氢氧化钠溶液浓度保持在1.8mol/L。
HIGHLIGHTS(1) The characteristics of glass and polypropylene diffusion dishes and their effects on the determination of soil hydrolysable nitrogen were compared.
(2) The use of a polypropylene diffusion dish and the improvement of the vessel cleaning method and sealing performance improve the stability of hydrolysable nitrogen determination and the convenience of experimental operation.
(3) For the determination of hydrolysable nitrogen in soil samples, reducing agent should be added, and the concentration of sodium hydroxide solution should be kept at 1.8mol/L.
Abstract:BACKGROUNDThe traditional alkaline hydrolysis diffusion separation acid-base titration method is used to determine the hydrolysable nitrogen in soil samples. Usually, a glass diffusion dish is used for alkaline hydrolysis diffusion separation. However, during sample pretreatment and alkaline hydrolysis diffusion separation, the operator often faces the following three problems. First, the solution in the inner chamber of the glass diffusion dish is very easily polluted by sodium hydroxide solution and alkaline glue solution. Second, ammonia leakage occurs easily between the glass diffusion dish and the cover, and it is often not possible to remedy when it is found. Third, the glass diffusion dish is bulky and fragile, and the experimental operation is inconvenient, all of which lead to the instability of measurement results due to inexperience of the operator.
OBJECTIVESTo establish a new method for the determination of hydrolysable nitrogen in soil samples by alkaline hydrolysis diffusion separation acid-base titration based on polypropylene diffusion dish.
METHODSA polypropylene diffusion dish was used instead of a glass diffusion dish in the alkaline hydrolysis of hydrolysable nitrogen. The cleaning method and the sealing of the diffusion dish were improved. The addition amount of reducing agent and the concentration of sodium hydroxide solution (1.8mol/L) were unified. The addition volume of sodium hydroxide solution was appropriately increased, and the concentration of hydrochloric acid standard solution was reduced.
RESULTSThe absolute deviation of reference materials GBW07416a with the measured value of hydrolysable nitrogen < 50mg/kg was 0.2-1.8mg/kg. The absolute deviation of reference materials GBW07415a, NSA-1, NSA-4, NSA-5 and NSA-6 with the measured value of hydrolysable nitrogen of 50-200mg/kg was 0-4.0mg/kg. The recovery rate of nitrate nitrogen converted to ammonium nitrogen by reducing agent was 89.6%-96.4%. The measured value of soil available reference materials was consistent with the standard value.
CONCLUSIONSThe stability and accuracy of hydrolysable nitrogen determination are improved. The pollution in this method is significantly reduced, ammonia leakage is avoided, and the operation is convenient. The method meets the requirements for determining the content of hydrolysable nitrogen in soil samples.

-
土壤水解性氮,又称土壤有效氮,包括铵态氮、硝态氮、比较简单的氨基酸氮、酰胺以及易水解蛋白质氮[1],是《土地质量地球化学评价规范》(DZ/T 0295—2016)土壤养分重要评价指标之一,除了可以为农田修复[2]、城市绿地土壤修复及质量评价[3-4]、生态地球化学调查[5]、生态风险评价[6]等重点调查项目推进提供基础数据支撑,还可以为综合肥力评价[7]、土壤养分优化[8]、土壤耕层重构[9]、区域施肥管理体系的构建[10]、生态涵养区开发[11]等常规项目开发提供重要信息,甚至可以为研究农作物品质与地球化学条件的关系[12]、沙化草地根系分布与土壤理化性质的相关性学术研究[13]等提供参考信息。因此,建立准确测定土壤样品中水解性氮含量的方法对于开展土地退化评估和实施修复性土地管理措施[14]和相关科学研究具有重要意义。
目前,土壤样品中水解性氮的测定方法有近红外光谱法[15-16]、碱解蒸馏分离-酸碱滴定法[17]和碱解扩散分离-酸碱滴定法[18-22]。近红外光谱法的操作比较简单,在野外快速测定碱解氮含量时使用较多,但该法易受土壤样品颗粒分布不均匀和粒径大小影响而产生漫射,往往需要进行多元漫射校正等一系列操作才能得到近似的数值,因此存在测定结果不准确的问题。碱解蒸馏分离-酸碱滴定法虽然能够把土壤样品中水解性氮全部蒸馏并测定出来,但该法一方面在蒸馏时需要用到高温水蒸气,可能会额外蒸馏出一些常温下难以水解的蛋白质氮,导致测定结果不同程度地偏高;另一方面,该法由于缺乏行业标准和国家标准依据,测定结果的可靠性难以保证。目前,基于玻璃扩散皿的碱解扩散分离-酸碱滴定法仍是测定土壤样品中水解性氮的主要方法。该法碱解温度较低,碱解过程平缓,既能把土壤样品中水解性氮充分碱解分离出来,又不易分离出其他干扰成分,因此水解性氮测定结果准确性较好。但是,玻璃扩散皿内外室在碱解过程中容易发生相互污染[18],毛玻璃盖在碱解过程中容易移位造成漏气,可能导致测定结果偏高或者偏低[22]。同时,玻璃扩散皿偏重偏脆也严重影响了操作便捷性。
本文采用聚丙烯扩散皿代替玻璃扩散皿对土壤中的水解性氮进行碱解,扩散分离出来的氨气用硼酸-指示剂溶液吸收,然后用盐酸标准溶液滴定硼酸-指示剂溶液得出水解性氮含量。通过对实验中的还原剂、氢氧化钠溶液浓度和体积、碱解时间、盐酸标准溶液等可能对土壤样品水解性氮测定结果造成影响的因素进行优化,对清洗扩散皿的方法和盖严扩散皿的操作进行改进,提升了土壤中水解性氮测定结果的准确性和稳定性。使用土壤有效态标准物质GBW07415a、GBW07416a、NSA-1、NSA-4、NSA-5、NSA-6对本文方法进行验证,其水解性氮测定结果的绝对偏差均满足《森林土壤氮的测定》(LY/T 1228—2015)的要求,由此建立了测定土壤样品中水解性氮的可行方法。
1. 实验部分
1.1 仪器及工作条件
电子天平:ML204/02型,梅特勒-托利多仪器(上海)有限公司,精确到万分之一克。
聚丙烯扩散皿:外径90mm,杭州优肯化工仪器有限公司,可使用温度范围为-30~140℃,在80℃以下能耐酸、碱、盐液的腐蚀。工作温度40℃。
电热恒温鼓风干燥箱:UP-GZ-9240B型,四川优浦达科技有限公司,控温范围为10~300℃,可精确到0.1℃。工作温度40℃。
半微量滴定管:容量10mL,天津市天波玻璃仪器制造有限公司,最小分度值为0.05mL。
1.2 材料和主要试剂
阿拉伯树胶粉:纯度不少于99%,购自天津市瑞金特化学品有限公司。
无水碳酸钾:优级纯,购自成都市科隆化学品有限公司。
碱性胶液:称取400g阿拉伯树胶粉和500mL高纯水于烧杯中,调匀,水浴加热到70℃后,冷却。加入400mL丙三醇和200mL饱和碳酸钾水溶液,搅匀,冷却,离心除去不溶物后,置于干燥器中。碱性胶液可以一次配好,能长期使用。
盐酸(优级纯)、七水合硫酸亚铁(分析纯)、氢氧化钠(分析纯):均购自西陇科学股份有限公司。
硼酸:优级纯;丙三醇:优级纯;甲基红、溴甲酚绿:均购自天津市科密欧化学试剂有限公司。
锌粉:锌含量99.99%,600目,购自上海阿拉丁生化科技股份有限公司。
超纯水:电阻率为18.25MΩ·cm。
0.005 mol/L硼砂标准溶液:称取9.534g硼砂,用超纯水定容到500mL容量瓶中,摇匀,获得0.1mol/L硼砂溶液,记为溶液B;移取10mL溶液B,用超纯水定容至200mL容量瓶中,获得0.005mol/L硼砂标准溶液。
甲基红-溴甲酚绿混合指示剂:称取0.10g甲基红并研磨细后,与0.50g溴甲酚绿一起溶解于100mL 95%乙醇中,摇匀。此试剂有效期2个月。
0.005 mol/L盐酸标准溶液:量取8.4mL盐酸,用超纯水定容至1L,摇匀,获得0.1mol/L盐酸溶液,记为溶液A;移取50mL溶液A,用超纯水定容至1000mL容量瓶中, 摇匀,获得0.005mol/L盐酸标准溶液。此盐酸标准溶液每次使用前均需用0.005mol/L硼砂标准溶液标定。
标定:吸取20.0mL 0.005mol/L硼砂标准溶液于250mL锥形瓶中,加1滴甲基红-溴甲酚绿混合指示剂,用0.005mol/L盐酸标准溶液滴定至溶液由蓝色变成紫红色终点。同时做空白实验。盐酸标准溶液的浓度(c,mol/L)按下式计算:
$$ c=\frac{c_1 \times V_1}{V_2-V_0} $$ (1) 式中:c1—硼砂标准溶液浓度(mol/L);V1—硼砂标准溶液体积(mL);V2—盐酸标准溶液体积(mL);V0—空白试验消耗盐酸标准溶液体积(mL)。
20g/L硼酸-指示剂溶液:称取20.0g硼酸溶于1L水中,摇匀。使用前,每升硼酸溶液中加5.0mL甲基红-溴甲酚绿混合指示剂,再用0.1mol/L氢氧化钠溶液调节pH至4.5,现配现用。
1.8 mol/L氢氧化钠溶液:称取72.0g氢氧化钠溶于高纯水,定容至1L,摇匀。
锌-硫酸亚铁还原剂:称取50.0g经磨细并过60目筛网的七水合硫酸亚铁和10.0g锌粉,混匀,储存于棕色瓶中,保存期限不超过7天。
1.3 实验样品
土壤有效态成分分析标准物质GBW07415a、GBW07416a,以及农业土壤有效态成分分析参比标准物质NSA-1、NSA-4、NSA-5、NSA-6均购自中国地质科学院地球物理地球化学勘查研究所。上述土壤标准物质包含了具有代表性的水稻土、红壤、黑土、紫色土。
用于统计的样品来自云南、青海和内蒙古自治区的部分农耕区,采样深度20cm,采集回来的土壤样品置于风干盘中,平铺成薄层,自然晾干,除去杂质后充分混匀,过10目筛后备测。上述区域样品有红壤、水稻土、紫色土、石灰土、冲积土、草甸土、黑钙土、栗钙土、灌淤土、棕钙土、潮土,涵盖了大部分常见的土壤类型。
1.4 实验方法
分别称取1.0000g(精确至0.0001g)过2mm筛的风干土壤样品和1g锌-硫酸亚铁还原剂并混匀,均匀地平铺于聚丙烯扩散皿外室。加4.0mL 20g/L硼酸-指示剂溶液于聚丙烯扩散皿内室,在聚丙烯扩散皿外室边缘上方涂碱性胶液。盖上盖子,使盖子与聚丙烯扩散皿外室边缘上方碱性胶液略微粘合,然后稍微打开盖子一侧,使聚丙烯扩散皿与盖子之间露出一条狭缝。往该狭缝加入15.0mL 1.8mol/L氢氧化钠溶液,立即盖严盖子并用橡皮筋交叉成十字形圈紧。将盖好的聚丙烯扩散皿置于电热恒温鼓风干燥箱中,于40℃碱解24h后,揭开聚丙烯扩散皿盖子,用0.005mol/L盐酸标准溶液滴定,聚丙烯扩散皿内室液体颜色由蓝色变为紫红色即到滴定终点,同时进行样品空白实验和标准物质实验。
水解性氮含量(wN,mg/kg)按下式计算:
$$ w_{\mathrm{N}}=\frac{\left(V-V_0\right) \times c \times 14}{m \times k_1} \times 10^3 $$ (2) 式中:V—滴定样品所用盐酸标准溶液体积(mL);V0—滴定空白所用盐酸标准溶液体积(mL);c—盐酸标准溶液的浓度(mol/L);m—风干土壤样品的质量(g);k1—由风干土壤样品换算成烘干土壤样品的水分换算系数;14—氮原子的摩尔质量(g/mol)。
2. 结果与讨论
2.1 扩散皿材质的选择
学者们[23-27]在研究不同材质、不同结构扩散皿对水解性氮测定结果影响时发现,使用塑料扩散皿测定土壤样品中水解性氮的精密度优于使用玻璃扩散皿的精密度,并且经过高强度使用后仍可保持较好的气密性,碱解扩散分离-酸碱滴定法水解性氮测定结果与扩散皿材质、规格、设计、内壁深度有关。本文随机抽取外观大小一致的不同材质扩散皿各20个,分别对比了它们的内壁深度与质量,聚丙烯扩散皿内壁深度在1.8~1.9cm,内壁与扩散皿底部垂直,玻璃扩散皿内壁深度在1.2~1.6cm,内壁与扩散皿底部呈斜坡状;聚丙烯扩散皿质量在37.2~38.2g,玻璃扩散皿质量在187~277g。显然,对于两种外观一致的扩散皿,聚丙烯扩散皿往往内壁更深,质量更轻,彼此差异更小,因此,理论上更不容易被外室氢氧化钠溶液污染,操作更加便捷,对水解性氮测定结果的绝对偏差影响更小。
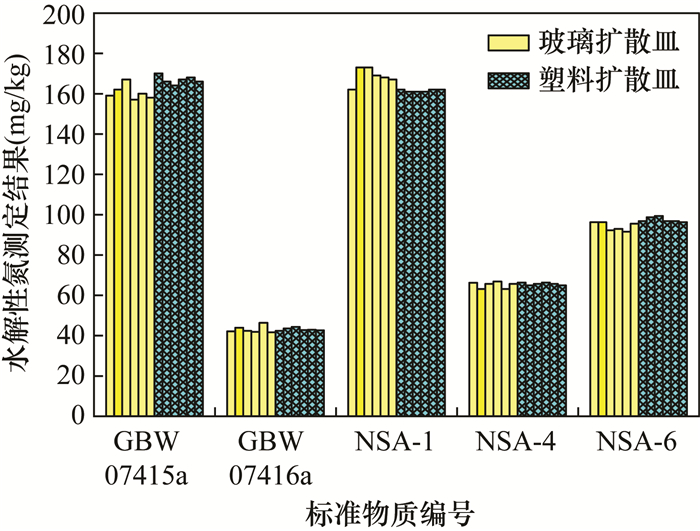
为进一步考察两种材质扩散皿对水解性氮测定结果的影响,采用1.4节实验方法,选取土壤有效态成分分析标准物质GBW07415a、GBW07416a和农业土壤有效态成分分析参比标准物质NSA-1、NSA-4、NSA-6,用两种材质扩散皿分别进行6份平行实验,标准物质水解性氮测定结果见图 1。对比图 1中两种不同材质扩散皿不同标准物质平行实验结果之间波动趋势,聚丙烯扩散皿的结果波动趋于平缓,玻璃扩散皿的测定结果波动较为明显,且呈无规律状态,可见,聚丙烯扩散皿的测定结果稳定性更好,本实验结论与前人[23-25]的对比实验结论一致。由于聚丙烯材质的韧性和可塑性好,在实际应用中,一方面,聚丙烯扩散皿因变形而损坏的数量远远小于玻璃扩散皿因磕碰而损坏的数量;另一方面,将聚丙烯扩散皿盖子设计成带凸起卡环的形状,可从根本上杜绝扩散皿和盖子在保温过程中可能出现移位、造成漏气使结果偏低的情形。显然,聚丙烯扩散皿比玻璃扩散皿更为适用。
2.2 预防聚丙烯扩散皿内室污染的措施
一些学者[20-21, 27-28]在分析中发现,少量样品因操作不慎进入扩散皿内室和少量氢氧化钠溶液溅入内室,均会造成污染影响测定结果,但上述两种情况在常温下清洗干净较为容易。最难消除的污染是碱性胶液在常温下难以清洗干净而可能带来的交叉污染。可采取的措施是:每次使用聚丙烯扩散皿和盖子之前,先用毛刷和自来水将其刷洗干净,然后用沸水煮半个小时,取出冷却后,用10%盐酸浸泡1h,取出,用高纯水冲洗,自然晾干后才可使用;当聚丙烯扩散皿涂抹碱性胶液后,往聚丙烯扩散皿内室加入4mL硼酸-指示剂溶液再观察15min,如果酒红色硼酸-指示剂溶液无污染,按正常进行下一步操作,如出现蓝绿色污染现象,将被污染的硼酸-指示剂溶液弃去,再次往聚丙烯扩散皿内室加入4mL硼酸-指示剂溶液,观察有无污染。如有污染,重复弃去和加入硼酸-指示剂溶液操作,直至整个聚丙烯扩散皿内室液面均呈酒红色,再进行下一步操作。
2.3 碱解过程中还原剂和氢氧化钠溶液对水解性氮测定的影响
还原剂的作用是将硝态氮转化为铵态氮。张英利等[29]对硝态氮的加标回收率实验证明了还原剂是有能力将水溶液中硝态氮完全转化为铵态氮。为进一步验证锌-七水合硫酸亚铁还原剂对土壤样品中硝态氮的还原能力,本文将稀硝酸钾溶液定量加入到常用的不同类型土壤有效态标准物质中,按照1.4节实验方法进行加标回收率实验,实验结果见表 1。不同类型土壤有效态标准物质中硝态氮加标回收率在89.6%~96.4%之间,证明了锌-七水合硫酸亚铁还原剂是有能力将土壤有效态样品中的硝态氮完全还原成铵态氮。
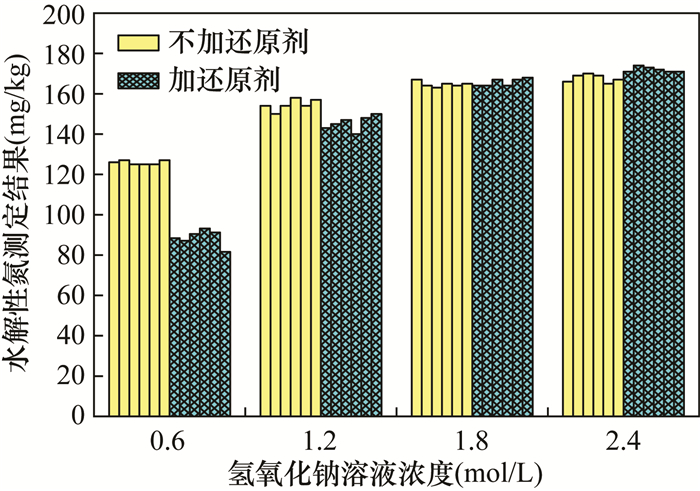
表 1 不同类型土壤有效态标准物质中硝态氮的加标回收率(n=6)Table 1. Recovery rate of nitrate nitrogen in available reference materials of different types of soil (n=6)样品名称 水解性氮标准值(mg/kg) 未加标样品水解性氮测定值(mg/kg) 加标量(以硝酸钾中氮元素含量计,μg) 加标样品水解性氮测定值(mg/kg) 加标回收率(%) GBW07415a(水稻土) 165±10 168 166 321 92.2 NSA-1(黑土) 166±7 166 166 326 96.4 NSA-4(紫色土) 64±4 63.9 69.2 130 95.5 NSA-6(红壤) 96±7 95.5 111 195 89.6 孔凡伟等[21]和童娟等[27]对可能影响水解性氮测定结果的各种因素进行了系统性研究,认为水稻土样品可用1.2mol/L氢氧化钠溶液,不加还原剂。本文选择土壤有效态成分分析标准物质GBW07415a(湖北水稻土),采用1.4节实验方法考察不同氢氧化钠溶液浓度下,是否加入还原剂对水解性氮测定的影响,每种情形均做6份平行实验,测定结果统计如图 2所示。实验表明当氢氧化钠溶液浓度为1.8mol/L时,是否加入还原剂,对水解性氮测定结果无影响;当氢氧化钠溶液浓度降低至1.2mol/L或0.6mol/L时,不加还原剂时水解性氮测定结果都高于加还原剂的测定结果。但无论是否加入还原剂,GBW07415a样品中大部分水解性氮测定结果已经超出《森林土壤氮的测定》(LY/T 1228—2015)中水解性氮测定值允许偏差的要求。因此,建议所有土壤有效态样品,只要是涉及测定土壤水解性氮,均加还原剂,氢氧化钠溶液浓度均保持在1.8mol/L。
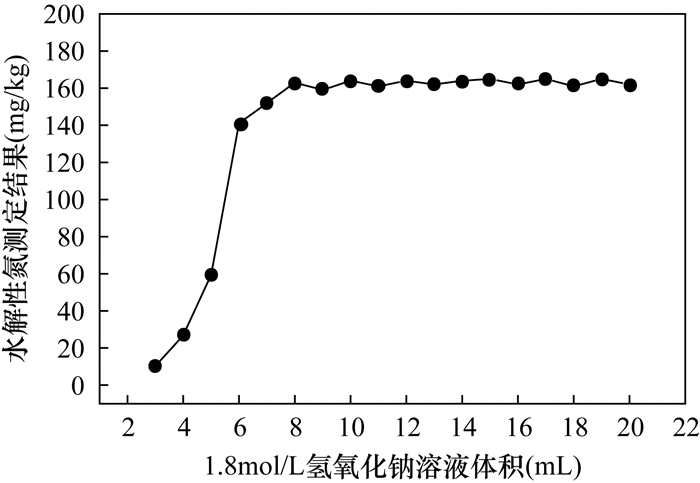
为考察氢氧化钠溶液加入体积对水解性氮测定的影响,选择土壤有效态成分分析标准物质GBW07415a,按照1.4节实验方法进行实验,只改变加入氢氧化钠溶液的体积,该标准物质水解性氮测定结果随氢氧化钠溶液加入体积的变化如图 3所示。结果表明,当加入氢氧化钠溶液体积达8mL以上,水解性氮测定结果趋于平稳;再增加氢氧化钠溶液的体积,对水解性氮测定结果不会造成影响。
但是,实际土壤样品往往比标准物质更为复杂,并且由于只经过10目筛,其颗粒远大于经过80目筛的标准物质颗粒[30],土壤样品平铺于扩散皿外室过程中,时常有部分样品会附着于扩散皿壁上,如果加入氢氧化钠溶液过少,这部分样品很难润湿到,通过摇动或者水平转动扩散皿虽然可以增强润湿效果,但也增加了扩散皿内外室的交叉污染风险。实验发现,当加入氢氧化钠溶液体积增加至15mL时,氢氧化钠在自然状态下恰好可以润湿所有样品,同时因不必摇动扩散皿而减少了污染的风险。因此,选择氢氧化钠溶液加入体积为15mL。
2.4 影响氨气泄漏的主要因素及应对措施
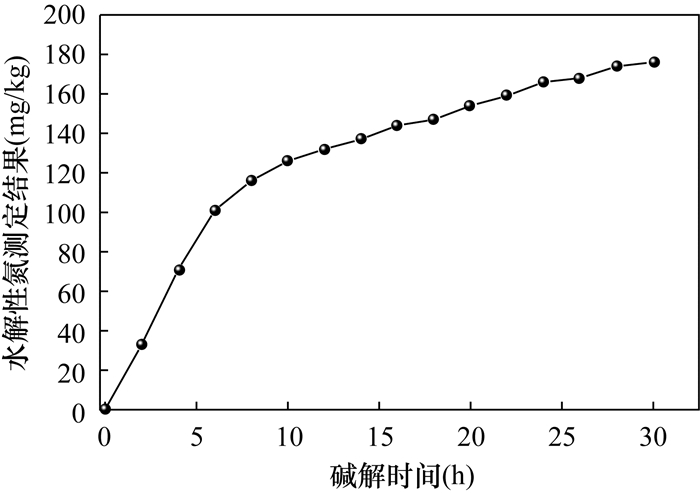
侯建伟等[26]研究认为,往扩散皿外室加入氢氧化钠溶液后,需要尽快盖严盖子,否则会导致氨气挥发,最终引起土壤水解性氮的测定值小于实际值。为了考察氨气在整个碱解过程中挥发的特点,本文选择土壤有效态成分分析标准物质GBW07415a,采用1.4节实验方法,只改变碱解时间,得出30h内水解性氮测定结果随碱解时间变化情况如图 4所示。结果表明,氨气在碱解过程中挥发是一个持续而长期的过程。可见,扩散皿与盖子合上瞬间,氨气挥发量很少,对水解性氮测定结果的影响可忽略不计,此时的操作不应追求尽快,而是以稳为主,避免污染。在24h碱解过程中,出现持续的氨气泄漏,才是影响水解性氮测定结果偏低的主要因素。为了防止碱解过程中氨气持续泄漏,一方面,聚丙烯扩散皿长期使用后,如果出现严重形变导致气密性不严的,应及时剔除;另一方面,要避免出现扩散皿与盖子之间碱性胶液过少导致粘合不严,进而出现持续氨气泄漏的情况。因此,涂抹好碱性胶液后,盖上盖子时,盖子与扩散皿外室边缘上方碱性胶液达到略微粘合即可,然后稍微打开盖子一侧,使扩散皿与盖子之间露出一条狭缝,往该狭缝加入15.0mL 1.8mol/L氢氧化钠溶液,立即盖严盖子并用橡皮筋交叉成十字形圈紧。经过大量实践验证,此操作可以有效地防止24h碱解过程中的氨气泄漏。
2.5 盐酸标准溶液浓度的选择
行业标准LY/T 1228—2015中水解性氮的测定使用的盐酸标准溶液浓度为0.01mol/L,李星等[31]使用的盐酸标准溶液浓度为0.005mol/L。本文认为盐酸标准溶液浓度的选择,一方面受需要滴定土壤样品中水解性氮含量范围的影响,另一方面需要尽可能地降低方法检出限和测定下限,以满足低含量水解性氮土壤样品分析的需要。
据测量和计算,聚丙烯扩散皿内室能接受最大滴定体积为17mL,10mL半微量滴定管200滴酸液实际体积为7mL,计算出最小液滴体积为0.035mL。根据《环境监测分析方法标准制订技术导则》(HJ 168—2020)附录A中滴定法检出限(MDL,mg/kg)计算公式:
$$ \mathrm{MDL}=k \lambda \frac{\rho V_0 M_1}{M_0 V_1} $$ (3) 式中:λ—被测组分与滴定液的摩尔比;ρ—滴定液的质量浓度(g/mL);V0—滴定管所产生的最小液滴体积(mL);M0—滴定液的摩尔质量(g/moL);V1—被测组分的取样体积(mL);M1—被测项目的摩尔质量(g/moL);k—当为一次滴定时,k=1。
以4倍检出限对应的浓度作为测定下限。可推导出不同盐酸标准溶液浓度可滴定水解性氮的最大含量,对应的方法检出限和测定下限列于表 2。
表 2 不同浓度盐酸标准溶液的滴定结果及对应的方法特性指标Table 2. Titration results of different concentrations of hydroric acid standard solutions and corresponding method characteristic indexes盐酸标准溶液浓度(mol/L) 可滴定水解性氮最大含量wN(mg/kg) 方法检出限MDL(mg/kg) 测定下限(mg/kg) 0.002 476 0.74 2.94 0.005 1190 1.84 7.35 0.01 2380 3.68 14.7 在《土地质量地球化学评价规范》(DZ/T 0295—2016)附录D土壤中养分等级划分中,按照水解性氮含量将水解性氮的养分等级总共分为五等:一等(>150mg/kg)为丰富;二等(大于120~150mg/kg)为较丰富;三等(大于90~120mg/kg)为中等;四等(大于60~90mg/kg)为较缺乏;五等(≤60mg/kg)为缺乏。显然,盐酸标准溶液浓度为0.002mol/L、0.005mol/L、0.010mol/L都能满足该规范要求。
考虑到不同地区土壤样品类型比较复杂,需要测定的水解性氮含量范围可能会更宽,通过对来自云南、青海和内蒙古自治区部分农耕区大量土壤样品进行统计学分析发现,一般土壤样品水解性氮含量分布在25~400mg/kg,少量土壤样品接近900mg/kg,当盐酸标准溶液浓度为0.005mol/L时,可滴定土壤样品中水解性氮含量范围是0~1190mg/kg,可以满足各类土壤样品中不同含量范围水解性氮分析的需要,并且该分析方法检出限为1.84mg/kg,测定下限为7.35mg/kg,对于土壤样品中水解性氮含量在20mg/kg左右的低含量样品是一个比较合适的选择。综合考虑,选择盐酸标准溶液浓度为0.005mol/L。
2.6 分析方法比对
2.6.1 绝对偏差和允许偏差
按照1.4节实验方法,选择土壤有效态标准物质GBW07415a、GBW07416a和农业土壤有效态参比标准物质NSA-1、NSA-4、NSA-5、NSA-6分别平行测定6次。表 3结果表明各标准物质中水解性氮测定结果的绝对偏差均满足《森林土壤氮的测定》(LY/T 1228—2015)中水解性氮测定结果允许偏差的要求,表明该方法准确、可靠。
表 3 土壤有效态标准物质水解性氮测定结果的绝对偏差和允许偏差Table 3. Absolute deviation and allowable deviation of determination results of hydrolysable nitrogen in soil available standard materials标准物质编号 土壤类型 水解性氮标准值(mg/kg) 水解性氮测定值(mg/kg) 水解性氮测定平均值(mg/kg) 绝对偏差(mg/kg) LY/T 1228—2015允许偏差(mg/kg) GBW07415a 水稻土 165±10 169 167 2.0 绝对偏差10~2.5 GBW07415a 水稻土 165±10 166 1.0 绝对偏差10~2.5 GBW07415a 水稻土 165±10 171 4.0 绝对偏差10~2.5 GBW07415a 水稻土 165±10 164 3.0 绝对偏差10~2.5 GBW07415a 水稻土 165±10 167 0 绝对偏差10~2.5 GBW07415a 水稻土 165±10 165 2.0 绝对偏差10~2.5 GBW07416a 红壤 44±4 42.9 43.4 0.5 绝对偏差 < 2.5 GBW07416a 红壤 44±4 42.7 0.7 绝对偏差 < 2.5 GBW07416a 红壤 44±4 45.2 1.8 绝对偏差 < 2.5 GBW07416a 红壤 44±4 43.8 0.4 绝对偏差 < 2.5 GBW07416a 红壤 44±4 43.2 0.2 绝对偏差 < 2.5 GBW07416a 红壤 44±4 42.5 0.9 绝对偏差 < 2.5 NSA-1 黑土 166±7 163 163 0 绝对偏差10~2.5 NSA-1 黑土 166±7 167 4.0 绝对偏差10~2.5 NSA-1 黑土 166±7 165 2.0 绝对偏差10~2.5 NSA-1 黑土 166±7 162 1.0 绝对偏差10~2.5 NSA-1 黑土 166±7 159 4.0 绝对偏差10~2.5 NSA-1 黑土 166±7 163 0 绝对偏差10~2.5 NSA-4 紫色土 64±4 62.5 62.2 0.3 绝对偏差10~2.5 NSA-4 紫色土 64±4 64.2 2.0 绝对偏差10~2.5 NSA-4 紫色土 64±4 61.7 0.5 绝对偏差10~2.5 NSA-4 紫色土 64±4 61.4 0.8 绝对偏差10~2.5 NSA-4 紫色土 64±4 62.2 0 绝对偏差10~2.5 NSA-4 紫色土 64±4 60.9 1.3 绝对偏差10~2.5 NSA-5 水稻土 180±10 174 176 2.0 绝对偏差10~2.5 NSA-5 水稻土 180±10 178 2.0 绝对偏差10~2.5 NSA-5 水稻土 180±10 176 0 绝对偏差10~2.5 NSA-5 水稻土 180±10 175 1.0 绝对偏差10~2.5 NSA-5 水稻土 180±10 175 1.0 绝对偏差10~2.5 NSA-5 水稻土 180±10 179 3.0 绝对偏差10~2.5 NSA-6 红壤 96±7 97.3 98.2 0.9 绝对偏差10~2.5 NSA-6 红壤 96±7 99.2 1.0 绝对偏差10~2.5 NSA-6 红壤 96±7 98.8 0.6 绝对偏差10~2.5 NSA-6 红壤 96±7 100 1.8 绝对偏差10~2.5 NSA-6 红壤 96±7 94.4 3.8 绝对偏差10~2.5 NSA-6 红壤 96±7 99.5 1.3 绝对偏差10~2.5 2.6.2 不同方法间的比对与综合评价
为综合评价几种常见碱解蒸馏-酸碱滴定法和碱解扩散分离-酸碱滴定法的优势与不足,实验梳理并对比了5种不同方法的相对标准偏差、相对误差、方法优势与存在问题,详细信息见表 4。可以看出,碱解扩散分离-酸碱滴定法与碱解蒸馏-酸碱滴定法的水解性氮测定结果整体是可靠的,但碱解扩散分离-酸碱滴定法测定值整体上更加接近标准值,可能与该法中水解性氮的碱解比较完全,同时碱解过程比较温和,其他形态氮不容易被碱解出来、干扰比较少有关,但该法流程整体偏长;碱解蒸馏-酸碱滴定法操作简单,但准确度稍差,可能与高温蒸馏时碱解出一些难溶的蛋白质氮造成结果偏高有关;基于玻璃扩散皿的碱解扩散分离-酸碱滴定法虽然结果准确,但稳定性不足,这可能与玻璃扩散皿材质及设计有关,导致该法在实验操作和碱解过程中容易受污染和发生氨气泄漏。
表 4 土壤中水解性氮测定的不同测定方法比对与综合评价Table 4. Comparison and comprehensive evaluation of different methods used in determination of hydrolysable nitrogen in soil测定方法名称 相对标准偏差RSD(%) 相对误差(%) 方法优势 存在问题 参考文献 基于塑料带孔扩散皿的碱解扩散分离-酸碱滴定法 1.63~3.19 0~2.28 无碱性胶液,精密度和准确度好 碱解过程中,如果发生氨气泄漏无法被发现 [24] 基于玻璃扩散皿的碱解扩散分离-酸碱滴定法 3.09~5.47 1.23~2.42 准确度好 扩散皿内室容易被污染,密封性不强,测定结果不够稳定 [20] 基于乳胶塞注射式玻璃扩散皿的碱解扩散分离-酸碱滴定法 1.97~2.84 0.61~2.46 精密度和准确度好,密封性好 扩散皿内室容易被污染,需额外操作注射器 [26] 基于FOSS Kjeltec 8400凯氏定氮仪碱解蒸馏-酸碱滴定法 1.10~2.13 3.40~7.33 操作简单,精密度较高,抗污染能力强 高温蒸馏,测定结果可能偏高 [17] 基于聚丙烯扩散皿的碱解扩散分离-酸碱滴定法(本文方法) 1.56~2.30 1.21~1.40 精密度和准确度好,密封性好 流程偏长 本文 总的来说,本文建立的基于聚丙烯扩散皿的碱解扩散分离-酸碱滴定法虽然流程偏长,但聚丙烯塑料不易被碱污染,同时经过有针对性的设计加强了扩散皿碱解过程中的密封性,水解性氮结果的稳定性和准确性得到了有效提升。
3. 结论
针对应用碱解扩散分离-酸碱滴定法测定土壤水解性氮测定结果准确性好,但是存在稳定性不足的问题,本文从改变扩散皿材质、改善扩散皿清洗方法、优化涂抹碱性胶液方式、还原剂和氢氧化钠溶液加入量等方面进行实验,从测定结果来看,改善扩散皿清洗方法、对还原剂和氢氧化钠加入量进行统一都达到了预期目的,但改变扩散皿材质和优化涂抹碱性胶液的操作,还不能完全降低污染和减少氨气在碱解过程中的泄漏问题。总体上,本文建立的基于聚丙烯扩散皿的碱解扩散分离-酸碱滴定法测定土壤水解性氮,碱解比较彻底,不会引入其他形态氮,滴定过程简单,测定结果能满足土地质量地球化学调查和区域性生态地球化学调查土壤样品中水解性氮测定的要求。
为实现本文方法没有任何污染和氨气泄漏的目标,今后一方面尝试对扩散皿进行全新设计,最终达到扩散皿中的氢氧化钠溶液在前处理过程中即使剧烈晃动也无法溅入内室,另一方面继续探索相关途径使扩散皿在整个碱解过程中完全密封,并从根本上杜绝使用碱性胶液,进一步提高水解性氮测定结果的准确性和稳定性。
-
表 1 不同类型土壤有效态标准物质中硝态氮的加标回收率(n=6)
Table 1 Recovery rate of nitrate nitrogen in available reference materials of different types of soil (n=6)
样品名称 水解性氮标准值(mg/kg) 未加标样品水解性氮测定值(mg/kg) 加标量(以硝酸钾中氮元素含量计,μg) 加标样品水解性氮测定值(mg/kg) 加标回收率(%) GBW07415a(水稻土) 165±10 168 166 321 92.2 NSA-1(黑土) 166±7 166 166 326 96.4 NSA-4(紫色土) 64±4 63.9 69.2 130 95.5 NSA-6(红壤) 96±7 95.5 111 195 89.6 表 2 不同浓度盐酸标准溶液的滴定结果及对应的方法特性指标
Table 2 Titration results of different concentrations of hydroric acid standard solutions and corresponding method characteristic indexes
盐酸标准溶液浓度(mol/L) 可滴定水解性氮最大含量wN(mg/kg) 方法检出限MDL(mg/kg) 测定下限(mg/kg) 0.002 476 0.74 2.94 0.005 1190 1.84 7.35 0.01 2380 3.68 14.7 表 3 土壤有效态标准物质水解性氮测定结果的绝对偏差和允许偏差
Table 3 Absolute deviation and allowable deviation of determination results of hydrolysable nitrogen in soil available standard materials
标准物质编号 土壤类型 水解性氮标准值(mg/kg) 水解性氮测定值(mg/kg) 水解性氮测定平均值(mg/kg) 绝对偏差(mg/kg) LY/T 1228—2015允许偏差(mg/kg) GBW07415a 水稻土 165±10 169 167 2.0 绝对偏差10~2.5 GBW07415a 水稻土 165±10 166 1.0 绝对偏差10~2.5 GBW07415a 水稻土 165±10 171 4.0 绝对偏差10~2.5 GBW07415a 水稻土 165±10 164 3.0 绝对偏差10~2.5 GBW07415a 水稻土 165±10 167 0 绝对偏差10~2.5 GBW07415a 水稻土 165±10 165 2.0 绝对偏差10~2.5 GBW07416a 红壤 44±4 42.9 43.4 0.5 绝对偏差 < 2.5 GBW07416a 红壤 44±4 42.7 0.7 绝对偏差 < 2.5 GBW07416a 红壤 44±4 45.2 1.8 绝对偏差 < 2.5 GBW07416a 红壤 44±4 43.8 0.4 绝对偏差 < 2.5 GBW07416a 红壤 44±4 43.2 0.2 绝对偏差 < 2.5 GBW07416a 红壤 44±4 42.5 0.9 绝对偏差 < 2.5 NSA-1 黑土 166±7 163 163 0 绝对偏差10~2.5 NSA-1 黑土 166±7 167 4.0 绝对偏差10~2.5 NSA-1 黑土 166±7 165 2.0 绝对偏差10~2.5 NSA-1 黑土 166±7 162 1.0 绝对偏差10~2.5 NSA-1 黑土 166±7 159 4.0 绝对偏差10~2.5 NSA-1 黑土 166±7 163 0 绝对偏差10~2.5 NSA-4 紫色土 64±4 62.5 62.2 0.3 绝对偏差10~2.5 NSA-4 紫色土 64±4 64.2 2.0 绝对偏差10~2.5 NSA-4 紫色土 64±4 61.7 0.5 绝对偏差10~2.5 NSA-4 紫色土 64±4 61.4 0.8 绝对偏差10~2.5 NSA-4 紫色土 64±4 62.2 0 绝对偏差10~2.5 NSA-4 紫色土 64±4 60.9 1.3 绝对偏差10~2.5 NSA-5 水稻土 180±10 174 176 2.0 绝对偏差10~2.5 NSA-5 水稻土 180±10 178 2.0 绝对偏差10~2.5 NSA-5 水稻土 180±10 176 0 绝对偏差10~2.5 NSA-5 水稻土 180±10 175 1.0 绝对偏差10~2.5 NSA-5 水稻土 180±10 175 1.0 绝对偏差10~2.5 NSA-5 水稻土 180±10 179 3.0 绝对偏差10~2.5 NSA-6 红壤 96±7 97.3 98.2 0.9 绝对偏差10~2.5 NSA-6 红壤 96±7 99.2 1.0 绝对偏差10~2.5 NSA-6 红壤 96±7 98.8 0.6 绝对偏差10~2.5 NSA-6 红壤 96±7 100 1.8 绝对偏差10~2.5 NSA-6 红壤 96±7 94.4 3.8 绝对偏差10~2.5 NSA-6 红壤 96±7 99.5 1.3 绝对偏差10~2.5 表 4 土壤中水解性氮测定的不同测定方法比对与综合评价
Table 4 Comparison and comprehensive evaluation of different methods used in determination of hydrolysable nitrogen in soil
测定方法名称 相对标准偏差RSD(%) 相对误差(%) 方法优势 存在问题 参考文献 基于塑料带孔扩散皿的碱解扩散分离-酸碱滴定法 1.63~3.19 0~2.28 无碱性胶液,精密度和准确度好 碱解过程中,如果发生氨气泄漏无法被发现 [24] 基于玻璃扩散皿的碱解扩散分离-酸碱滴定法 3.09~5.47 1.23~2.42 准确度好 扩散皿内室容易被污染,密封性不强,测定结果不够稳定 [20] 基于乳胶塞注射式玻璃扩散皿的碱解扩散分离-酸碱滴定法 1.97~2.84 0.61~2.46 精密度和准确度好,密封性好 扩散皿内室容易被污染,需额外操作注射器 [26] 基于FOSS Kjeltec 8400凯氏定氮仪碱解蒸馏-酸碱滴定法 1.10~2.13 3.40~7.33 操作简单,精密度较高,抗污染能力强 高温蒸馏,测定结果可能偏高 [17] 基于聚丙烯扩散皿的碱解扩散分离-酸碱滴定法(本文方法) 1.56~2.30 1.21~1.40 精密度和准确度好,密封性好 流程偏长 本文 -
[1] 吴昊, 朱红霞, 袁懋, 等. 气相分子吸收光谱法测定土壤中铵态氮和硝态氮[J]. 岩矿测试, 2021, 40(1): 165-171. doi: 10.15898/j.cnki.11-2131/td.202003100029 Wu H, Zhu H X, Yuan M, et al. Determination of ammonium nitrogen and nitrate in soil by gas phase molecular absorption spectrometry[J]. Rock and Mineral Analysis, 2021, 40(1): 165-171. doi: 10.15898/j.cnki.11-2131/td.202003100029
[2] 李义纯, 王艳红, 陈勇, 等. 基于土壤质量的改良剂修复镉污染稻田综合效果评价[J]. 农业环境科学学报, 2021, 40(6): 1219-1228. https://www.cnki.com.cn/Article/CJFDTOTAL-NHBH202106012.htm Li Y C, Wang Y H, Chen Y, et al. A comprehensive evaluation of remediation effects on cadmium contamination in paddy fields based on soil quality[J]. Journal of Agro-Environment Science, 2021, 40(6): 1219-1228. https://www.cnki.com.cn/Article/CJFDTOTAL-NHBH202106012.htm
[3] 王红, 徐静, 谢晓金, 等. 南京市绿地土壤养分特征及空间分布[J]. 江苏农业科学, 2021, 49(6): 212-218. https://www.cnki.com.cn/Article/CJFDTOTAL-JSNY202106039.htm Wang H, Xu J, Xie X J, et al. Characteristics and spatial distribution of soil nutrients in green space in Nanjing City[J]. Jiangsu Agricultural Sciences, 2021, 49(6): 212-218. https://www.cnki.com.cn/Article/CJFDTOTAL-JSNY202106039.htm
[4] 程晓月, 许宏刚, 朱亚灵, 等. 兰州市中心城区道路绿地土壤pH和养分特征[J]. 草业科学, 2021, 38(3): 468-479. https://www.cnki.com.cn/Article/CJFDTOTAL-CYKX202103007.htm Cheng X Y, Xu H G, Zhu Y L, et al. Study on soil pH and nutrients in a roadside green belt in a central urban area of Lanzhou[J]. Pratacultural Science, 2021, 38(3): 468-479. https://www.cnki.com.cn/Article/CJFDTOTAL-CYKX202103007.htm
[5] 代杰瑞, 庞绪贵, 刘华峰, 等. 山东省东部地区农业生态地球化学调查及生态问题浅析[J]. 岩矿测试, 2012, 31(1): 189-197. http://www.ykcs.ac.cn/cn/article/id/ykcs_20120128 Dai J R, Pang X G, Liu H F, et al. Agro-ecological geochemical survey and evaluation of eastern Shandong Province[J]. Rock and Mineral Analysis, 2012, 31(1): 189-197. http://www.ykcs.ac.cn/cn/article/id/ykcs_20120128
[6] 贺灵, 孙彬彬, 吴超, 等. 浙江省江山市猕猴桃果园土壤环境质量与生态风险评价[J]. 岩矿测试, 2019, 38(5): 524-533. doi: 10.15898/j.cnki.11-2131/td.201901080003 He L, Sun B B, Wu C, et al. Assessment of soil environment quality and ecological risk for kiwifruit orchards in Jiangshan City, Zhejiang Province[J]. Rock and Mineral Analysis, 2019, 38(5): 524-533. doi: 10.15898/j.cnki.11-2131/td.201901080003
[7] 王杰, 张春燕, 卢加文, 等. 广安区柑橘土壤养分状况及综合肥力评价[J]. 土壤通报, 2021, 52(6): 1360-1367. https://www.cnki.com.cn/Article/CJFDTOTAL-TRTB202106011.htm Wang J, Zhang C Y, Lu J W, et al. Nutrient status and comprehensive fertility evaluation of the citrus soil in Guang'an District[J]. Chinese Journal of Soil Science, 2021, 52(6): 1360-1367. https://www.cnki.com.cn/Article/CJFDTOTAL-TRTB202106011.htm
[8] 曹胜, 周卫军, 刘沛, 等. 冰糖橙果园土壤养分与果实品质关系的多元分析及优化方案[J]. 土壤, 2021, 53(1): 97-104. https://www.cnki.com.cn/Article/CJFDTOTAL-TURA202101013.htm Cao S, Zhou W J, Liu P, et al. Multivariate analysis and optimization of relationship between soil nutrients and fruit quality in C. sinensis(L. ) osbeck orchard[J]. Soils, 2021, 53(1): 97-104. https://www.cnki.com.cn/Article/CJFDTOTAL-TURA202101013.htm
[9] 邓小华, 何铭钰, 陈金, 等. 山地酸性土壤耕层重构的理化性状及酶活性动态变化[J]. 中国烟草科学, 2021, 42(4): 17-23. https://www.cnki.com.cn/Article/CJFDTOTAL-ZGYV202104003.htm Deng X H, He M Y, Chen J, et al. Dynamic of soil physi-chemical properties and enzymatic activities after restructured arable layer of mountainous acidic soil[J]. Chinese Tobacco Science, 2021, 42(4): 17-23. https://www.cnki.com.cn/Article/CJFDTOTAL-ZGYV202104003.htm
[10] 高宏艳, 索全义, 郑海春, 等. 基于GIS和丰缺指标法的区域施肥管理体系的构建[J]. 植物营养与肥料学报, 2021, 27(9): 1648-1655. https://www.cnki.com.cn/Article/CJFDTOTAL-ZWYF202109015.htm Gao H Y, Suo Q Y, Zheng H C, et al. Construction of regional fertilization system based on GIS and nutrient abundance index[J]. Journal of Plant Nutrition and Fertilizers, 2021, 27(9): 1648-1655. https://www.cnki.com.cn/Article/CJFDTOTAL-ZWYF202109015.htm
[11] 冯辉, 张学君, 张群, 等. 北京大清河流域生态涵养区富硒土壤资源分布特征和来源分析[J]. 岩矿测试, 2019, 38(6): 693-704. doi: 10.15898/j.cnki.11-2131/td.201905270071 Feng H, Zhang X J, Zhang Q, et al. Distribution characteristics and sources identification of selenium-rich soils in the ecological conservation area of the Daqinghe River watershed, Beijing[J]. Rock and Mineral Analysis, 2019, 38(6): 693-704. doi: 10.15898/j.cnki.11-2131/td.201905270071
[12] 顾涛, 朱晓华, 赵信文, 等. 广州新垦莲藕产区莲藕品质与地球化学条件的关系[J]. 岩矿测试, 2021, 40(6): 833-845. doi: 10.15898/j.cnki.11-2131/td.202109290136 Gu T, Zhu X H, Zhao X W, et al. Relationship between lotus root quality and geochemical conditions in the Xinken lotus root producing area of Guangzhou[J]. Rock and Mineral Analysis, 2021, 40(6): 833-845. doi: 10.15898/j.cnki.11-2131/td.202109290136
[13] 周启龙. 藏西沙化草地根系分布与土壤理化性质的关系[J]. 水土保持通报, 2021, 41(1): 1-5. https://www.cnki.com.cn/Article/CJFDTOTAL-STTB202101001.htm Zhou Q L. Relation between root distribution character-istics and soil physical and chemical properties in desertification grassland in western Tibet[J]. Bulletin of Soil and Water Conservation, 2021, 41(1): 1-5. https://www.cnki.com.cn/Article/CJFDTOTAL-STTB202101001.htm
[14] 粮农组织.《世界粮食和农业领域土地及水资源状况: 系统濒临极限》2021年概要报告[R/OL]. https://doi.org/10.4060/cb7654en. Food and Agriculture Organization.The state of the world's land and water resources for food and agriculture-systems at breaking point.Synthesis Report 2021.Rome[R/OL]. https://doi.org/10.4060/cb7654en.
[15] 吴金卓, 孔琳琳, 李颖, 等. 近红外光谱法测定土壤全氮和碱解氮含量[J]. 湖南农业大学学报(自然科学版), 2016, 42(1): 91-96. https://www.cnki.com.cn/Article/CJFDTOTAL-HNND201601019.htm Wu J Z, Kong L L, Li Y, et al. Prediction models of total and available soil nitrogen based on near-infrared spectroscopy[J]. Journal of Hunan Agricultural University (Natural Sciences), 2016, 42(1): 91-96. https://www.cnki.com.cn/Article/CJFDTOTAL-HNND201601019.htm
[16] 彭海根, 金楹, 詹莜国, 等. 近红外光谱技术结合竞争自适应重加权采样变量选择算法快速测定土壤水解性氮含量[J]. 分析测试学报, 2020, 39(10): 1305-1310. https://www.cnki.com.cn/Article/CJFDTOTAL-TEST202010021.htm Peng H G, Jin Y, Zhan Y G, et al. Quantitative determination of hydrolytic nitrogen content in soil by near infrared spectroscopy combined with competitive adaptive reweighted sampling variable selection algorithm[J]. Journal of Instrumental Analysis, 2020, 39(10): 1305-1310. https://www.cnki.com.cn/Article/CJFDTOTAL-TEST202010021.htm
[17] 石欣. 凯氏定氮仪测定土壤中水解性氮含量[J]. 宁夏农林科技, 2018, 59(11): 55-58. https://www.cnki.com.cn/Article/CJFDTOTAL-NXNL201811020.htm Shi X. Determination of hydrolytic nitrogen content in soil by Kjeltec nitrogen analyzer[J]. Ningxia Journal of Agriculture and Forestry Science and Technology, 2018, 59(11): 55-58. https://www.cnki.com.cn/Article/CJFDTOTAL-NXNL201811020.htm
[18] 王晓岚, 卡丽毕努尔, 杨文念. 土壤碱解氮测定方法比较[J]. 北京师范大学学报(自然科学版), 2010, 46(1): 76-78. https://www.cnki.com.cn/Article/CJFDTOTAL-BSDZ201001021.htm Wang X L, Ka L B N E, Yang W N. Comparison of methods for determining alkali-hydrolyzed nitrogen in soil[J]. Journal of Beijing Normal University (Natural Science), 2010, 46(1): 76-78. https://www.cnki.com.cn/Article/CJFDTOTAL-BSDZ201001021.htm
[19] 莎娜, 张三粉, 骆洪, 等. 两种土壤碱解氮测定方法的比较[J]. 内蒙古农业科技, 2014(6): 25-33. https://www.cnki.com.cn/Article/CJFDTOTAL-NMGN201406013.htm Sha N, Zhang S F, Luo H, et al. Comparison two kinds of determination method of soil alkaline hydrolysis nitrogen[J]. Inner Mongolia Agricultural Science and Technology, 2014(6): 25-33. https://www.cnki.com.cn/Article/CJFDTOTAL-NMGN201406013.htm
[20] 魏娜. 两种土壤碱解氮测定方法比较[J]. 西藏农业科技, 2014, 36(1): 30-34. https://www.cnki.com.cn/Article/CJFDTOTAL-XZNY201401008.htm Wei N. Comparison between two methods of available nitrogen in soil[J]. Tibet Journal of Agricultural Sciences, 2014, 36(1): 30-34. https://www.cnki.com.cn/Article/CJFDTOTAL-XZNY201401008.htm
[21] 孔凡伟. 简述土壤水解氮的测定方法[J]. 黑龙江农业科学, 2010(4): 159-160. https://www.cnki.com.cn/Article/CJFDTOTAL-HLJN201004059.htm Kong F W. The determination method briefly introduced of soil hydrolyzed nitrogen[J]. Heilongjiang Agricultural Sciences, 2010(4): 159-160. https://www.cnki.com.cn/Article/CJFDTOTAL-HLJN201004059.htm
[22] 贺毅. 扩散法测定土壤中的水解性氮[J]. 华北自然资源, 2020(2): 95-100. https://www.cnki.com.cn/Article/CJFDTOTAL-HBGT202002036.htm He Y. Determination of hydrolytic nitrogen in soil by diffusion method[J]. Huabei Natural Resources, 2020(2): 95-100. https://www.cnki.com.cn/Article/CJFDTOTAL-HBGT202002036.htm
[23] 施畅, 万秋月, 秦冲, 等. 塑料密封盒-滴定法测定土壤中碱解氮[J]. 中国无机分析化学, 2017, 7(3): 33-37. https://www.cnki.com.cn/Article/CJFDTOTAL-WJFX201703011.htm Shi C, Wan Q Y, Qin C, et al. Determination of alkali-hydrolyzable nitrogen in soil by titration with a sealed plastic box[J]. Chinese Journal of Inorganic Analytical Chemistry, 2017, 7(3): 33-37. https://www.cnki.com.cn/Article/CJFDTOTAL-WJFX201703011.htm
[24] 杨清华. 森林土壤中水解性氮测定方法改进研究[J]. 现代农业科技, 2018(18): 131-132. https://www.cnki.com.cn/Article/CJFDTOTAL-ANHE201818078.htm Yang Q H. Improvement of determination method of hydrolytic nitrogen in forest soil[J]. Modern Agricultural Science and Technology, 2018(18): 131-132. https://www.cnki.com.cn/Article/CJFDTOTAL-ANHE201818078.htm
[25] 周剑. 塑料扩散皿在土壤水解性氮测定中的应用[J]. 福建地质, 2021, 40(1): 77-82. https://www.cnki.com.cn/Article/CJFDTOTAL-FJDZ202101009.htm Zhou J. Application of plastic diffusion dish in determination of hydrolytic in soil[J]. Geology of Fujian, 2021, 40(1): 77-82. https://www.cnki.com.cn/Article/CJFDTOTAL-FJDZ202101009.htm
[26] 侯建伟, 邢存芳, 杨莉琳. 土壤碱解氮测定方法优化改革[J]. 西南师范大学学报(自然科学版), 2021, 46(7): 45-49. https://www.cnki.com.cn/Article/CJFDTOTAL-XNZK202107006.htm Hou J W, Xing C F, Yang L L. Optimization reform of soil available nitrogen determination method[J]. Journal of Southwest China Normal University (Natural Science Edition), 2021, 46(7): 45-49. https://www.cnki.com.cn/Article/CJFDTOTAL-XNZK202107006.htm
[27] 童娟, 谢春梅. 碱解扩散法测定土壤水解性氮影响因素分析[J]. 宁夏农林科技, 2011, 52(9): 61-71. https://www.cnki.com.cn/Article/CJFDTOTAL-NXNL201109030.htm Tong J, Xie C M. Analysis on influencing factors of soil hydrolytic nitrogen determination by alkaline hydrolysis diffusion method[J]. Ningxia Journal of Agriculture and Forestry Science and Technology, 2011, 52(9): 61-71. https://www.cnki.com.cn/Article/CJFDTOTAL-NXNL201109030.htm
[28] 林晓峰. 土壤水解性氮含量的测定方法及注意事项[J]. 江西农业, 2017(11): 23-25. https://www.cnki.com.cn/Article/CJFDTOTAL-JXNG201711019.htm Lin X F. Determination method and precautions of soil hydrolytic nitrogen content[J]. Jiangxi Agriculture, 2017(11): 23-25. https://www.cnki.com.cn/Article/CJFDTOTAL-JXNG201711019.htm
[29] 张英利, 马爱生, 杨岩荣, 等. 不同还原剂对土壤碱解氮测定结果的影响[J]. 干旱地区农业研究, 2002, 20(2): 39-41. https://www.cnki.com.cn/Article/CJFDTOTAL-GHDQ200202009.htm Zhang Y L, Ma A S, Yang Y R, et al. Effect of different reductive on analysis results of soil available nitrogen[J]. Agricultural Research in the Arid Areas, 2002, 20(2): 39-41. https://www.cnki.com.cn/Article/CJFDTOTAL-GHDQ200202009.htm
[30] 刘妹, 顾铁新, 程志中, 等. 10个土壤有效态成分分析标准物质研制[J]. 岩矿测试, 2011, 30(5): 536-544. http://www.ykcs.ac.cn/cn/article/id/ykcs_20110503 Liu M, Gu T X, Cheng Z Z, et al. Ten reference materials for available nutrients of agricultural soils[J]. Rock and Mineral Analysis, 2011, 30(5): 536-544. http://www.ykcs.ac.cn/cn/article/id/ykcs_20110503
[31] 李星, 郭小彪, 张墨. 土壤中水解性氮的测定条件选择[J]. 北京农业, 2015(24): 73-74. https://www.cnki.com.cn/Article/CJFDTOTAL-BJNY201524040.htm Li X, Guo X B, Zhang M. Selection of determination conditions of hydrolytic nitrogen in soil[J]. Beijing Agriculture, 2015(24): 73-74. https://www.cnki.com.cn/Article/CJFDTOTAL-BJNY201524040.htm
-
期刊类型引用(3)
1. 张梓妍,郝运平,李荣慧,方美,耿丽娜. 氮掺杂荧光碳点的制备及其对MnO~-_4的检测. 河北师范大学学报(自然科学版). 2025(01): 70-76 .  百度学术
百度学术
2. 王肖文,吴文丽,杜文韬,钞瀚贤,陈建祥,丁明洁,李晓燕,李银峰. 氮掺杂碳点的制备及其在Hg~(2+)测定中的应用研究. 河南城建学院学报. 2024(03): 112-117 .  百度学术
百度学术
3. 鲁莉华,王辉,赵艳芳. γ-氨基丁酸修饰氧化石墨烯的合成及其应用. 实验室研究与探索. 2021(05): 5-8 .  百度学术
百度学术
其他类型引用(1)



 下载:
下载:
 京公网安备 11010202008159号
京公网安备 11010202008159号